题目内容
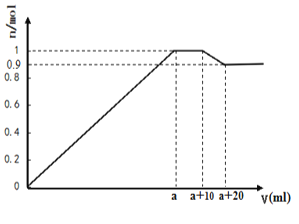
【题目】在一定体积的含有Al3+、Mg2+、Ba2+的混合溶液中逐滴加入NaOH和Na2SO4的混合溶液(除上述离子外,其他离子不与所加试剂反应,假设Al3+、Mg2+结合OH-的能力相同),产生沉淀的物质的量与所加溶液的体积的关系如图所示。下列说法正确的是:
A. 当a<V<a+10时,不再生成难溶物
B. 上述含Al3+、Mg2+、Ba2+的混合溶液中3c(Al3+)+2c(Mg2+)=c(Ba2+)
C. 上述含Al3+、Mg2+、Ba2+的混合溶液中n(Al3+) = 0.2mol
D. NaOH和Na2SO4的混合溶液中c(NaOH)>c(Na2SO4)
【答案】C
【解析】
在一定体积的含有Al3+、Mg2+、Ba2+的混合溶液中逐滴加入NaOH和Na2SO4的混合溶液,0~a mL时,图像为一条倾斜直线,可以推得生成Al(OH)3、Mg(OH)2、BaSO4沉淀,在a mL到(a+10)mL之间,图像为一条水平直线,可以推得沉淀一边生成一边溶解,且溶解的Al(OH)3和生成的BaSO4物质的量相等,则c(NaOH)=c(Na2SO4)。在(a+10)mL到(a+20)mL之间,沉淀一直溶解,反应为:Al(OH)3+OH-=AlO2-+2H2O,据此分析;
A.a mL到(a+10)mL之间,包含Al(OH)3的溶解和BaSO4的生成,故A项错误;
B.由图可知,当Al3+、Mg2+沉淀完全时,Ba2+还未沉淀完全,且NaOH和Na2SO4的混合溶液中c(NaOH)=c(Na2SO4),则3c(Al3+)+2c(Mg2+)<c(Ba2+),故B项错误;
C.在(a+10)mL到(a+20)mL之间,沉淀一直溶解,反应为:Al(OH)3+OH-=AlO2-+2H2O,可以看出滴加10mL混合溶液有0.1molAl(OH)3溶解,同理在a mL到(a+10)mL之间滴加10mL混合溶液也有0.1molAl(OH)3溶解,所以一共有0.2molAl(OH)3溶解,可以推得混合溶液中n(Al3+) = 0.2mol,故C项正确;
D.在a mL到(a+10)mL之间,图像为一条水平直线,可以推得沉淀一边生成一边溶解,且溶解的Al(OH)3和生成的BaSO4物质的量相等,则c(NaOH)=c(Na2SO4),故D项错误;
综上,本题选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某实验小组用 0.50 mol/L NaOH 溶液和 0.50 mol/L 硫酸溶液在如下图所示的装置中 进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
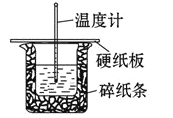
(1)从实验装置上看,图中缺少的一种玻璃仪器是_____。
(2)烧杯间填满碎纸条的作用是_____。
(3)若大烧杯上不盖硬纸板,求得的反应热数值______填“偏大”“偏小”或“无影响”)。
(4)若取取 50 mL NaOH 溶液和 30 mL 硫酸溶液进行实验,实验数据如下表。
温度 实验次数 | 起始温度 t1/℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 30.1 |
2 | 27.0 | 27.4 | 27.2 | 33.3 |
3 | 25.9 | 25.9 | 25.9 | 29.8 |
4 | 26.4 | 26.2 | 26.3 | 30.4 |
近似认为 0.50 mol/L NaOH 溶液和 0.50 mol/L 硫酸溶液的密度都是 1 g/cm3,中和后生成溶液 的比热容 c=4.18 J/(g·℃)。则中和热△H=_____(取小数点后一位)。