题目内容
17.下列化学式既能表示物质的组成,又能表示物质的一个分子的是( )| A. | NaCl | B. | C | C. | Fe | D. | Ar |
分析 化学式既能表示物质的组成,又能表示物质的一个分子的应是分子晶体物质,晶体中含有单个分子,而离子晶体、原子晶体和金属晶体无单个分子.
解答 解:A、NaCl为离子晶体,化学式为晶体中阴阳离子的个数比,晶体中不含单个分子,故A错误;
B、C是碳的化学式,它是由碳原子直接构成的,不能表示物质的一个分子,故B错误;
C、Fe为金属晶体,晶体中存在金属阳离子和自由移动的电子,不能存在分子,故C错误;
D、Ar是氩的化学式,是单原子分子,能表示一个Ar分子,故D正确; 故选D.
点评 本题考查晶体类型的判断,题目难度不大,注意只有分子晶体才含有单个分子,化学式即分子式.

练习册系列答案
相关题目
7.150ml 1mol/L的NaOH溶液吸收了2.24L CO2(标准状况下)则下列说法正确的是( )
| A. | HCO3-离子略多于CO32-离子 | |
| B. | HCO3-离子等于CO32-离子 | |
| C. | HCO3-离子略少于CO32-离子 | |
| D. | Na+离子数等于HCO3-和CO32-离子数之和 |
12.下列说法与事实不符合的是( )
| A. | 酯类化合物存在于许多水果中 | |
| B. | 大量含磷的生活污水排放有利于自然水体中鱼类的繁衍 | |
| C. | 碘化银可用于人工降雨 | |
| D. | 使用含碘食盐可以预防“大脖子病” |
8.某小组利用如图装置,用苯与溴在FeBr3催化作用下制备溴苯:

反应剧烈进行,烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现,蒸馏水逐渐变成黄色.反应停止后按 如下流程分离产品:

已知:
(1)操作Ⅰ为过滤,操作Ⅱ为蒸馏.
(2)“水洗”、“NaOH溶液洗”需要用到的玻璃仪器是分液漏斗、烧杯.
(3)“水洗”主要目的是除去FeBr3,“NaOH溶液洗”主要目的是除去Br2.
(4)锥形瓶中蒸馏水变黄的原因是溶解了从烧瓶中挥发出的溴.
(5)已知苯与溴发生的是取代反应,推测反应后锥形瓶中液体含有的两种大量离子是Br-、H+,请设计实验方案验证你的推测.(限选试剂:镁条、四氯化碳、氯水、溴水、蒸馏水)

反应剧烈进行,烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现,蒸馏水逐渐变成黄色.反应停止后按 如下流程分离产品:

已知:
| 沸点℃ | 密度g/cm3 | 溶解性 | |
| 溴 | 59 | 3.119 | 水中溶解度小,易溶于有机溶剂 |
| 苯 | 80 | 0.8765 | 难溶于水,与有机溶剂互溶 |
| 溴苯 | 156 | 1.50 | 难溶于水,与有机溶剂互溶 |
(2)“水洗”、“NaOH溶液洗”需要用到的玻璃仪器是分液漏斗、烧杯.
(3)“水洗”主要目的是除去FeBr3,“NaOH溶液洗”主要目的是除去Br2.
(4)锥形瓶中蒸馏水变黄的原因是溶解了从烧瓶中挥发出的溴.
(5)已知苯与溴发生的是取代反应,推测反应后锥形瓶中液体含有的两种大量离子是Br-、H+,请设计实验方案验证你的推测.(限选试剂:镁条、四氯化碳、氯水、溴水、蒸馏水)
| 序号 | 实验步骤 | 预期现象 | 结论 |
| 1 | 将锥形瓶中液体转入分液漏斗,加入适量四氯化碳,振荡后分液.分别取少量上层无色溶液于试管A、B中 | ||
| 2 | 锥形瓶中液体含大量 Br- | ||
| 3 | 锥形瓶中液体含大量 H+ |
 ;
;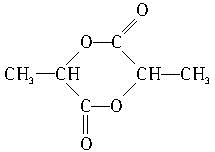 .
.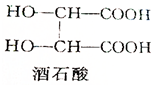 酒石酸的结构简式如图所示,它是葡萄酒中主要的有机酸之一,其主要用途是作饮料添加剂.写出酒石酸的分子式C4H6O6.
酒石酸的结构简式如图所示,它是葡萄酒中主要的有机酸之一,其主要用途是作饮料添加剂.写出酒石酸的分子式C4H6O6.