题目内容
4.下列转化及解释均正确的是( )| 转化 | 解释 | |
| A | CuS+H2SO4=CuSO4+H2S↑ | 酸性:H2SO4>H2S |
| B | AgCl(s)+I-(aq)?AgI(s)+Cl-(aq) | Kap(AgCl)<Kap(AgI) |
| C | 2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3;Fe+S$\frac{\underline{\;加热\;}}{\;}$FeS | 氧化性:Cl2>S |
| D | C(s,石墨)=C(s,金刚石)△H=+1.9kL/mol | 稳定性:石墨<金刚石 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.CuS与硫酸不反应;
B.发生沉淀的转化,向溶度积更小的方向移动;
C.不同氧化剂与变价金属反应,生成高价金属化合物对应的非金属性强;
D.能量低的物质稳定.
解答 解:A.CuS与硫酸不反应,也不能利用CuSO4与H2S的反应比较酸性,故A错误;
B.发生沉淀的转化,向溶度积更小的方向移动,则Kap(AgCl)>Kap(AgI),故B错误;
C.不同氧化剂与变价金属反应,生成高价金属化合物对应的非金属性强,可知Cl得到电子能力强,则氧化性:Cl2>S,故C正确;
D.由吸热反应可知,石墨能量低,则稳定性:石墨>金刚石,故D错误;
故选C.
点评 本题考查较综合,涉及难溶电解质的溶解平衡及转化、氧化性比较、稳定性比较,为高考常见的拼凑试题,把握物质的性质与反应原理为解答的关键,侧重分析与应用能力的考查,题目难度中等.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
3.化学与生活密切相关.下列应用中利用了物质氧化性的是( )
| A. | 明矾净化水 | B. | 纯碱去油污 | C. | 食醋除水垢 | D. | 漂白粉漂白织物 |
4.己烷雌酚的一种合成路线如图:下列叙述正确的是( )

| A. | 在NaOH水溶液中加热,化合物X可发生消去反应 | |
| B. | 在一定条件,化合物Y可与HCHO发生缩聚反应 | |
| C. | 用FeCl3溶液可鉴别化合物X和Y | |
| D. | 化合物Y中不含有手性碳原子 |
19.化学与日常生活密切相关.下列有关说法错误的是( )
| A. | 使用LED照明灯属于“低碳生活”方式 | |
| B. | 研制高性能的耐磨轮胎,可减少细颗粒物(PM2.5)的产生 | |
| C. | 在家用电热水器不锈钢内胆镶嵌镁棒,以防止内胆被侵蚀 | |
| D. | 施用适量石灰乳可降低盐碱地(含较多NaCl,Na2CO3)的碱性 |
9.X、Y、M、N是短周期主族元素,且原子序数依次增大.已知X原子的最外层电子数是电子层数的3倍,X、M同主族,Y原子在短周期主族元素中原子半径最大.下列说法不正确的是( )
| A. | M与X的化合物对应的水化物不一定都是强酸 | |
| B. | Y2X和Y2X2中化学键类型相同,阴、阳离子的个数比相同 | |
| C. | 气态氢化物的热稳定性:M<N | |
| D. | 离子半径r:r(X2-)>r(Y+) |
16.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=1的溶液中:Fe2+、Cl-、NO3-、K+ | |
| B. | 滴入酚酞显红色的溶液中:Na+、Al3+、CO32-、AlO2- | |
| C. | 加入铝粉产生H2的溶液中:Fe2+、Na+、SO42-、ClO- | |
| D. | 0.1mol•L-1 NaHCO3溶液中:Na+、NH4+、SO42-、NO3- |
14.用下列实验装置完成对应的实验,能达到实验目的且合理的是( )
| A. | 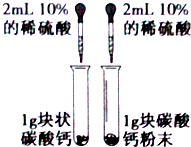 用图装置探究反应物接触面积对反应速率影响 | |
| B. | 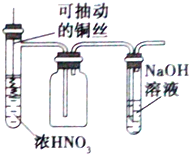 用图装置制取并收集少量的NO2气体(不考虑倒吸) | |
| C. |  用图装置制取并收集少量的氯气 | |
| D. |  用图装置制取少量乙酸乙酯 |
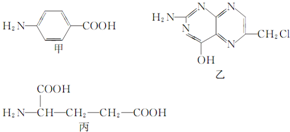 叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成.
叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成.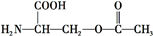 .
.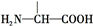
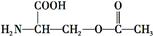 +2NaOH→HOCH2CH(NH2)COONa+H2O+CH3COONa.
+2NaOH→HOCH2CH(NH2)COONa+H2O+CH3COONa.