题目内容
11.设NA表示阿伏加德罗常数的值.下列说法正确的是( )| A. | 1 mol Cl2与足量的Fe充分反应,转移电子的数目为3NA | |
| B. | 常温下,1 L pH=1的H2SO4溶液中,由水电离出的H+数目为0.1NA | |
| C. | 常温下,21 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 1 mol ${\;}_{6}^{14}$C原子中所含中子数目为6NA |
分析 A、氯气与铁反应后变为-1价;
B、在硫酸溶液中,水的电离被抑制,氢离子几乎全部来自于酸的电离,OH-全部来自于水的电离;
C、乙烯和丁烯的最简式均为CH2;
D、根据中子数=质量数-质子数来计算.
解答 解:A、氯气与铁反应后变为-1价,则1mol氯气与铁反应会转移2mol电子,即2NA个,故A错误;
B、在硫酸溶液中,水的电离被抑制,氢离子几乎全部来自于酸的电离,OH-全部来自于水的电离,故水电离出的n(H+)=n(OH-)=10-13mol/L×1L=10-13mol,故水电离出的氢离子的个数为10-13NA,故B错误;
C、乙烯和丁烯的最简式均为CH2,故21g混合物中含有的CH2的物质的量n=$\frac{21g}{14g/mol}$=1.5mol,故含有的碳原子的物质的量为1.5mol,即1.5NA个,故C正确;
D、根据中子数=质量数-质子数可知,1 mol ${\;}_{6}^{14}$C原子中含8mol中子,即8NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握公式的运用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
20.下列关于物质的用途或说法不正确的是( )
| A. | 铝热反应原理是炼铁最常用的反应原理 | |
| B. | 氧化铝熔点很高,可用作耐火材料 | |
| C. | 过氧化钠可以用作呼吸面具中的供氧剂 | |
| D. | 青铜是我国使用最早的合金 |
2.设NA为阿付加德罗常数的值,下列说法正确的是( )
| A. | 1moL苯乙烯(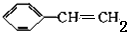 )中含有的碳酸双键数为4NA )中含有的碳酸双键数为4NA | |
| B. | 加热条件下,4.6g金属Na与足量O2反应的产物中阴离子的数目为0.1NA | |
| C. | 室温条件下,pH=9,体积为1L的CH4COONa溶液中,发生电离的水分子数为1.0×10-4NA | |
| D. | 高温条件下,16.6g铁粉与足量水蒸气反应后,转移电子数为0.9NA |
19.利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | 甲 | 乙 | 丙 | 实验结论 | 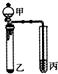 |
| A | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:碳>硅 | |
| B | 双氧水 | MnO2 | Na2S | 氧化性:H2O2>O2>S | |
| C | 浓硫酸 | Na2SO3 | 酸性KMnO4溶液 | SO2具有漂白性 | |
| D | 浓氨水 | 氢氧化钠固体 | 酚酞 | 碱性:NaOH>NH3•H2O |
| A. | A | B. | B | C. | C | D. | D |
6.用下列装置进行相应的实验,能实现预期目的是( )
| A | B | C | D | |
| 装置 |  |  H2(g)+I2(g)?2HI(g) | 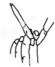 |  |
| 目的 | 检验碳与浓硫酸反应的氧化产物 | 验证压强对化学平衡的影响 | 检查碱式滴定管是否漏液 | FeSO4溶液的蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
16.某酸性溶液中加入Ba2+ 后出现白色沉淀,则该溶液中一定含有( )
| A. | Fe3+ | B. | SO42- | C. | NO3- | D. | Cl- |
3.化学与人类社会的生产、生活有着密切联系.下列叙述中正确的是( )
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 用活性炭为蔗糖脱色和用臭氧漂白纸浆,原理相似 | |
| C. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 | |
| D. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 |
20.酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是( )
| A. | 酯化反应的产物只有酯 | |
| B. | 酯化反应一般需要用NaOH溶液来吸收生成的酯 | |
| C. | 酯化反应是有限度的 | |
| D. | 浓硫酸可做酯化反应的催化剂 |
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 58 g乙烯和乙烷的混合气体中碳原子数目一定为4NA | |
| B. | 用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA | |
| C. | 142g Na2SO4和Na2HPO4固体混合物中,阴阳离子总数为3NA | |
| D. | 已知3BrF3+5H2O=HBrO3+Br2+9HF+O2↑ 如果有5mol H2O参加氧化还原反应,则由水还原的BrF3分子数目为3NA |