题目内容
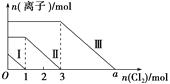
【题目】向仅含SO32-、I-、Br-且物质的量分别为m、n、6 mol 的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是( )
A.曲线Ⅱ代表Br-的变化情况
B.曲线Ⅰ对应的反应:SO32-+Cl2+H2O=2H++SO42-+2Cl-
C.通入的氯气为5 mol时,溶液中的主要阴离子为Cl-、SO32-
D.溶液中n(Na+)=n(SO32-)+n(I-)+n(Br-)
【答案】B
【解析】
向仅含SO32-、I-、Br-的溶液中通入适量氯气,还原性为SO32->I->Br-,首先发生反应H2O+SO32-+Cl2=SO42-+2Cl-+2H+,图中曲线I表示SO32-变化,然后发生2I-+Cl2=I2+2Cl-,故曲线II表示I-的变化,最后发生2Br-+Cl2=Br2+2Cl-,曲线III表示Br-的变化;
A.由上述分析可知,曲线II表示I-的变化,故A错误;
B.由还原性的强弱可知,曲线Ⅰ对应的反应:SO32-+Cl2+H2O═2H++SO42-+2Cl-,故B正确;
C.由图可知,通入的氯气为1 mol时,溶液中不存在SO32-,故C错误;
D.由电荷守恒可知,溶液中n(Na+)=2n(SO32-)+n(I-)+n(Br-),故D错误;
故答案为B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下表各组物质(或者它们的溶液)通过一步反应可实现如图所示的转化的是
选项 | X | Y | Z |
|
A | Si | Na2SiO3 | H2SiO3 | |
B | S | H2S | SO2 | |
C | Al2O3 | NaAlO2 | Al2(SO4)3 | |
D | Mg(OH)2 | MgCO3 | MgCl2 |
A.AB.BC.CD.D
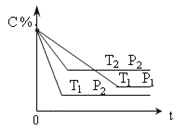
【题目】二氧化碳的回收利用对温室气体的减排具有重要的意义。在2L密闭容器中,加入2.00molCO2和2.0 mol H2以及催化剂发生反应:CO2(g)+H2 (g)![]() HCOOH(g) ΔH,测得,n(H2)/mol在不同温度随时间的变化如下表:
HCOOH(g) ΔH,测得,n(H2)/mol在不同温度随时间的变化如下表:
60 min | 90 min | 120 min | 150 min | 180 min | ||
实验I | Tl/K | 1.50 mol | 1.32 mol | 1.28 mol | 1.26 mol | 1.26 mol |
实验Ⅱ | T2/K | 1.45 mol | 1.20 mol | 1.10 mol | 1.10 mol | 1.10 mol |
(1)比较实验温度T1___T2(填“>”、“<”),该反应的ΔH___0(填“>”、“=”、“<”)。
(2)实验I中0~60 min内用HCOOH表示的该反应的平均反应速率为_____。
(3)实验Ⅱ反应开始时体系压强为P0,第90min时体系压强为Pl,则Pl∶P0=___。
(4)比较实验I、Ⅱ在80min时的逆反应速率大小vl___vⅡ(填“>”、“<”或“无法判断”),原因是_____。