题目内容
6.下列说法正确的是( )| A. | 根据醋酸溶液中分子和离子共存,即可证明溶液达到了电离平衡状态 | |
| B. | c(CH3COO-)=c(H+),则醋酸溶液达到电离平衡状态 | |
| C. | 当NH3•H2O达到电离平衡时,溶液中NH3•H2O和OH-的浓度肯定相等 | |
| D. | 磷酸是分步电离的,电离程度依次减弱 |
分析 A.无论是否达到平衡状态,CH3COOH、H+、CH3COO-都共存于同一溶液;
B.得到平衡状态时,各组分的浓度不变,不一定相等;
C.得到电离平衡状态时,一水合氨电离速率与生成一水合氨的速率相等,NH3•H2O和OH-的浓度不一定相等;
D.多元弱酸分步电离,且第一步电离产生的氢离子会抑制后来的电离过程.
解答 解:A.CH3COOH为弱电解质,在溶液中存在CH3COOH?CH3COO-+H+,当达到平衡状态时,各粒子的浓度恒定不变,而无论是否达到平衡状态,CH3COOH、H+、CH3COO-都共存,故A错误;
B.(CH3COO-)=c(H+),不能判断各组分的浓度是否发生变化,则无法判断醋酸溶液是否达到电离平衡状态,故B错误;
C.当溶液中NH3•H2O的电离速率等于合成NH3•H2O的速率时,达到电离了平衡状态,而此时NH3•H2O和OH-的浓度不一定相等,故C错误;
D.多元弱酸分步电离,且第一步电离产生的氢离子会抑制后来的电离过程,所以磷酸的电离程度依次减弱,故D正确;
故选D.
点评 本题考查了弱电解质的电离平衡状态的判断,题目难度中等,明确电离平衡状态的特征为解答关键,注意平衡时各组分浓度不变,不一定相等,为易错点,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
17.下列离子方程式书写正确的是( )
| A. | 钠和水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 碳酸钙和盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 三氯化铝加到过量的氨水中:Al3++3OH-═Al(OH)3↓ | |
| D. | 碳酸钠溶液与足量稀盐酸的反应:CO32-+2H+═H2O+CO2↑ |
14.地球环境日益恶化,为了保护环境人类正在尽力治理.下列说法正确的是 ( )
| A. | CO、甲苯、尼古丁等不是室内污染物 | |
| B. | 污水处理方法化学包括混凝法、中和法、沉淀法 | |
| C. | “白色污染”的会危及海洋生物的生存 | |
| D. | 垃圾资源化的方法是分类回收法 | |
| E. | 为防止流感传染,可将教室门窗关闭后,用甲醛熏蒸,进行消毒 | |
| F. | 铅笔芯的原料的重金属铅,儿童在使用时不可用嘴吮咬铅笔,以免引起铅中毒 | |
| G. | CO有毒,生有煤炉的居室,可放置数盆水这样可有效地吸收CO,以防煤气中毒 |
15.下列实验操作中不正确的是( )
| A. | 蒸发操作时,当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干 | |
| B. | 过滤后洗涤沉淀,是将水沿玻璃棒注入漏斗中,用玻璃棒搅拌后待水流下 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 萃取操作时,应选择有机萃取剂,它与原溶剂应不互溶 |
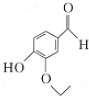 乙基香兰素是当今世界上最重要的合成香料之一,是食品添加剂中不可缺少的重要原料,其结构简式如图所示.
乙基香兰素是当今世界上最重要的合成香料之一,是食品添加剂中不可缺少的重要原料,其结构简式如图所示.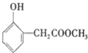 、
、 ;
;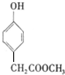 .
.
 .
.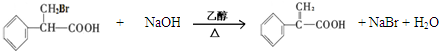 .
. .
.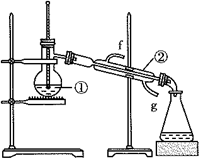 如图为蒸馏实验装置:
如图为蒸馏实验装置: