题目内容
1.请写出下列物质的电离方程式和离子方程式:(1)HCl:HCl=H++Cl-
(2)NaOH:NaOH=Na++OH-
(3)Na2CO3:Na2CO3=2Na++CO32-
(4)HCl和NaOH反应的离子方程式:H++OH-=H2O
(5)Ba(NO3)2和H2SO4反应的离子方程式:SO42-+Ba2+=BaSO4↓
(6)Na2CO3和HCl反应的离子方程式:CO32-+2H+=CO2↑+H2O.
分析 (1)(2)(3)中物质均为强电解质,完全电离,遵循电荷、原子守恒;
(4)反应生成氯化钠和水;
(5)反应生成硫酸钡和硝酸;
(6)反应生成氯化钠、水、二氧化碳,结合离子反应中保留化学式的物质书写离子反应方程式.
解答 解:(1)HCl的电离方程式为HCl=H++Cl-,故答案为:HCl=H++Cl-;
(2)NaOH的电离方程式为NaOH=Na++OH-,故答案为:NaOH=Na++OH-;
(3)Na2CO3的电离方程式为Na2CO3=2Na++CO32-,故答案为:Na2CO3=2Na++CO32-;
(4)HCl和NaOH反应的离子方程式为H++OH-=H2O,故答案为:H++OH-=H2O;
(5)Ba(NO3)2和H2SO4反应的离子方程式为SO42-+Ba2+=BaSO4↓,故答案为:SO42-+Ba2+=BaSO4↓;
(6)Na2CO3和HCl反应的离子方程式为CO32-+2H+=CO2↑+H2O,故A答案为:CO32-+2H+=CO2↑+H2O.
点评 本题考查电离方程式及离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
11.请按要求完成下列各小题:
(1)用CO2来生产燃料甲醇的反应原理为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g),某些化学键的键能数据如下表:
计算上述反应的焓变△H=(2d+3b-c-3a-3e)kJ/mol(用相应字母表示).写出上述反应的平衡常数表达式K=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$;若只加压,则平衡常数K不变(填“增大”“减小”或“不变”).
(2)在溶液中,NaH2PO4和Na3PO4等物质的量混合恰好完全反应,该反应的离子方程式为H2PO4-+PO43-=2HPO42-,
(3)某温度(t℃)时,测得0.01mol•L-1的NaOH溶液的pH=10.在此温度下,将0.01mol•L-1的H2SO4溶液VaL与P
H=12的NaOH溶液VbL混合,若所得混合液pH=11,则Va:Vb=15:2.
(4)在25℃时,将cmol•L-1的醋酸溶液与bmol•L-1NaOH溶液等体积混合后溶液刚好呈中性,用含b、c的代数式表示CH3COOH的电离常数Ka=$\frac{b×1{0}^{-7}}{c-b}$.
(5)三种弱酸HA、H2B、HC,电离平衡常数的数值为:①1.8×10-5、②5.6×10-11、③4.9×10-10、④4.3×10-2(数据顺序以打乱),已知三种酸和它们的盐之间能发生以下反应:HA+HB-(少量)=A-+H2B,H2B(少量)+C-=HB-+HC.则三种酸对应的电离平衡常数分别为(请用序号填空)
(1)用CO2来生产燃料甲醇的反应原理为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g),某些化学键的键能数据如下表:
| 化学键 | C-H | H-H | C-O | C=O | H-O |
| 键能/kj•mol-1 | a | b | c | d | e |
(2)在溶液中,NaH2PO4和Na3PO4等物质的量混合恰好完全反应,该反应的离子方程式为H2PO4-+PO43-=2HPO42-,
(3)某温度(t℃)时,测得0.01mol•L-1的NaOH溶液的pH=10.在此温度下,将0.01mol•L-1的H2SO4溶液VaL与P
H=12的NaOH溶液VbL混合,若所得混合液pH=11,则Va:Vb=15:2.
(4)在25℃时,将cmol•L-1的醋酸溶液与bmol•L-1NaOH溶液等体积混合后溶液刚好呈中性,用含b、c的代数式表示CH3COOH的电离常数Ka=$\frac{b×1{0}^{-7}}{c-b}$.
(5)三种弱酸HA、H2B、HC,电离平衡常数的数值为:①1.8×10-5、②5.6×10-11、③4.9×10-10、④4.3×10-2(数据顺序以打乱),已知三种酸和它们的盐之间能发生以下反应:HA+HB-(少量)=A-+H2B,H2B(少量)+C-=HB-+HC.则三种酸对应的电离平衡常数分别为(请用序号填空)
| HA | H2B | HC | ||
| Ka | Ka1 | Ka2 | Ka3 | Ka4 |
| 数值 | ||||
9.关于氨的下列叙述中,错误的是( )
| A. | 氨易液化,因此可用来作制冷剂 | |
| B. | 氨极易溶于水,因此可用来作喷泉实验 | |
| C. | 实验室制氨气的方法是加热NH4Cl | |
| D. | 液氨是纯净物 |
16.1997年,英国的“克隆羊”备受世界关注.“克隆羊”的关键技术之一是找到一些特殊的酶,这些酶能激活普通体细胞,使它像生殖细胞一样发育成个体.有关酶的叙述中错误的是( )
| A. | 酶是具有催化作用的蛋白质 | |
| B. | 酶的催化作用具有选择性和专一性 | |
| C. | 强酸性或强碱性条件下能降低酶的活性 | |
| D. | 使用热水和加酶洗衣粉能提去污能力 |
6.下列说法正确的是( )
| A. | 根据醋酸溶液中分子和离子共存,即可证明溶液达到了电离平衡状态 | |
| B. | c(CH3COO-)=c(H+),则醋酸溶液达到电离平衡状态 | |
| C. | 当NH3•H2O达到电离平衡时,溶液中NH3•H2O和OH-的浓度肯定相等 | |
| D. | 磷酸是分步电离的,电离程度依次减弱 |
13.为了除去铁粉中的少量铝粉,可以选取下列哪种溶液( )
| A. | 浓盐酸 | B. | 浓氢氧化钠溶液 | C. | 硫酸 | D. | 硝酸 |
11.用下列实验装置或操作进行的实验能达到实验目的是( )
| A. | 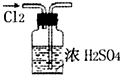 干燥Cl2 干燥Cl2 | B. | 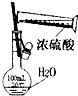 配制100ml 0.1mol•L-1硫酸溶液 | ||
| C. | 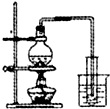 制取少量蒸馏水 | D. |  检验钾元素的存在 |