题目内容
17.下列离子方程式书写正确的是( )| A. | 钠和水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 碳酸钙和盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 三氯化铝加到过量的氨水中:Al3++3OH-═Al(OH)3↓ | |
| D. | 碳酸钠溶液与足量稀盐酸的反应:CO32-+2H+═H2O+CO2↑ |
分析 A.电子不守恒;
B.碳酸钙在离子反应中保留化学式;
C.一水合氨在离子反应中保留化学式;
D.反应生成氯化钠、水、二氧化碳.
解答 解:A.钠和水反应的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.碳酸钙和盐酸反应的离子反应为CaCO3+2H+═Ca2++CO2↑+H2O,故B错误;
C.三氯化铝加到过量的氨水中的离子反应为Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故C错误;
D.碳酸钠溶液与足量稀盐酸的反应的离子反应为CO32-+2H+═H2O+CO2↑,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列说法正确的是( )
| A. | 氯化钠和盐酸溶于水都发生电离,克服粒子间作用力的类型相同 | |
| B. | 氯化铵和水玻璃都属于离子化合物 | |
| C. | 直径介于1nm-10nm之间的微粒称为胶体 | |
| D. | 由IA族和VIA族元素可以形成含有原子个数比为l:1,离子个数比为2:l的离子化合物 |
5.下列关于化学反应的相关描述不正确的是( )
| A. | 胃舒平中含有氢氧化铝,可治疗胃酸过多:Al(OH)3+3HCl═AlCl3+3H2O | |
| B. | 碳铵是一种常用化肥,60℃分解完全:2NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O↑ | |
| C. | 生石灰可用作建筑材料:CaO+H2O=Ca(OH)2,属于化合反应 | |
| D. | 实验室常用氧化还原反应制备氧气:2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑ |
2.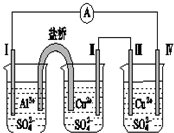 某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )
某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )
 某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )
某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )| A. | 电子方向:电极Ⅳ→→电极Ⅰ | B. | 电极Ⅰ发生还原反应 | ||
| C. | 电极Ⅱ逐渐溶解 | D. | 电极Ⅲ的电极反应:Cu-2e-═Cu2+. |
9.关于氨的下列叙述中,错误的是( )
| A. | 氨易液化,因此可用来作制冷剂 | |
| B. | 氨极易溶于水,因此可用来作喷泉实验 | |
| C. | 实验室制氨气的方法是加热NH4Cl | |
| D. | 液氨是纯净物 |
6.下列说法正确的是( )
| A. | 根据醋酸溶液中分子和离子共存,即可证明溶液达到了电离平衡状态 | |
| B. | c(CH3COO-)=c(H+),则醋酸溶液达到电离平衡状态 | |
| C. | 当NH3•H2O达到电离平衡时,溶液中NH3•H2O和OH-的浓度肯定相等 | |
| D. | 磷酸是分步电离的,电离程度依次减弱 |
7.下列关于药物的使用说法正确的是( )
| A. | 随着药店的普及,药物都可以直接去药店购买,不需要去医院 | |
| B. | 青霉素时一种常用药,感冒发烧、咳嗽肺炎都可以使用 | |
| C. | 长期大量使用阿司匹林可预防疾病,没有副作用 | |
| D. | 虽然药物能治病,但大部份药物有毒副作用 |