题目内容
【题目】可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空: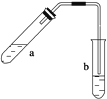
(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2 mL,正确的加入顺序及操作是?
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是?
(3)实验中加热试管a的目的是:
(4)试管b中加有饱和Na2CO3溶液,其作用是?
(5)反应结束后,振荡试管b,静置。观察到的现象是?
【答案】
(1)
先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,冷却后再加入冰醋酸
(2)
在试管a中加入几片沸石(或碎瓷片)
(3)
①加快反应速率②及时将产物乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向进行
(4)
吸收随乙酸乙酯蒸出的少量乙酸和乙醇并降低乙酸乙酯的溶解度
(5)
b中的液体分层,上层是透明的油状液体
【解析】 (1)浓H2SO4溶解时放出大量的热,因此应先加入乙醇然后边摇动试管边慢慢加入浓H2SO4 , 最后再加入冰醋酸。(2)为了防止发生暴沸应在加热前向试管中加入几片沸石(或碎瓷片)。(3)加热试管可提高反应速率,同时可将乙酸乙酯及时蒸出,有利于提高乙酸乙酯的产率。(4)乙酸乙酯在饱和Na2CO3溶液中溶解度很小,而随乙酸乙酯蒸出的乙酸和乙醇在其中的溶解度很大,因此便于分离出乙酸乙酯。(5)试管内液体分层,上层为油状液体,因为乙酸乙酯的密度小于水的密度。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目