题目内容
【题目】A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B、A与X均可形成10个电子化合物;B的最高价含氧酸可与其气态氢化物反应生成盐,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液先变红后褪色. 用元素符号或化学式回答下列问题.
(1)X在周期表中的位置是;
(2)化合物Y2X2的电子式为 , 它含有的化学键类型有(填序号). A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)X、Z的简单氢化物中沸点较高的是(填化学式),原因是 .
(4)A与X和A与Z均能形成18个电子的化合物,这两种化合物发生反应可生成Z,其反应的化学方程式为:;
(5)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则负极电极反应式为: .
【答案】
(1)第二周期第ⅥA族
(2)![]() ; AC
; AC
(3)H2O;水分子间存在氢键
(4)H2O2+H2S=S↓+2H2O
(5)H2﹣2e﹣+2OH﹣=2H2O
【解析】解:A、B、X、Y和Z是原子序数依次递增的短周期元素,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红,则Y2X2为Na2O2,X为O元素,Y为Na;X与Z同主族,则Z为S元素;B的最高价含氧酸可与其气态氢化物反应生成盐,则B为N元素;A与Y同主族,A与B、A与X均可形成10个电子化合物,则A为H元素.(1)X为O元素,在周期表中的位置是:第二周期第ⅥA族,
故答案为:第二周期第ⅥA族;(2)化合物Na2O2的电子式为 ![]() ,含有离子键、非极性共价键,
,含有离子键、非极性共价键,
故答案为: ![]() ;AC;(3)水分子间存在氢键,沸点高于硫化氢,
;AC;(3)水分子间存在氢键,沸点高于硫化氢,
故答案为:H2O;水分子间存在氢键;(4)H与O和H与S均能形成18个电子的化合物,这两种化合物发生反应可生成S,应是H2O2、H2S反应生成硫与水,反应的化学方程式为:H2O2+H2S=S↓+2H2O,
故答案为:H2O2+H2S=S↓+2H2O;(5)氢气、氧气制成新型的化学电源(KOH溶液作电解质溶液),负极发生氧化反应,氢气在负极失去电子,碱性条件下生成水,负极电极反应式为:H2﹣2e﹣+2OH﹣=2H2O,
故答案为:H2﹣2e﹣+2OH﹣=2H2O.
A、B、X、Y和Z是原子序数依次递增的短周期元素,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红,则Y2X2为Na2O2,X为O元素,Y为Na;X与Z同主族,则Z为S元素;B的最高价含氧酸可与其气态氢化物反应生成盐,则B为N元素;A与Y同主族,A与B、A与X均可形成10个电子化合物,则A为H元素.

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案【题目】下列实验的有关叙述错误的是( )
选项 | A | B | C | D |
实验装置图 |
|
|
|
|
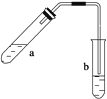
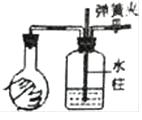
实验现象 | U形管右侧液面下降 | 小试管中品红溶液褪色 | 加入少量酚酞,溶液变浅红色 | 关闭弹簧夹,双手捂住圆底烧瓶,导管中水柱上升后静止不动 |
实验结论 | 该条件下铁钉发生吸氧腐蚀 | 证明二氧化硫具有还原性 | 证明Na2CO3能够发生水解 | 该装置气密性良好 |
A.A
B.B
C.C
D.D