题目内容
【题目】2013年,“雾霾”成为年度关键词.近年来,对“雾霾”的防护与治理成为越来越重要的环境问题和社会问题.雾霾主要由二氧化硫、氮氧化物和可吸入颗粒物这三项组成.
(1)机动车的尾气是雾霾形成的原因之一,近几年有人提出利用选择性催化剂利用汽油中挥发出来的C3H6催化还原尾气中的NO气体,请写出该过程的化学方程式:
(2)我国北方到了冬季烧煤供暖所产生的废气也是雾霾的主要来源之一.经研究发现将煤炭在O2/CO2的气氛下燃烧,发现能够降低燃煤时NO的排放,主要反应为:
2NO(g)+2CO(g)N2(g)+2CO2(g)△H
若①N2(g)+O2(g)2NO(g)△H1=+180.5kJmol﹣1
②CO(g)C(s)+ ![]() O2(g)△H2=+110.5kJmol﹣1
O2(g)△H2=+110.5kJmol﹣1
③C (s)+O2(g)CO2(g)△H3=﹣393.5kJmol﹣1
则△H=kJmol﹣1 .
(3)燃煤尾气中的SO2用NaOH溶液吸收形成NaHSO3溶液,在pH为4~7之间时电解,硫元素在铅阴极上被电解还原为Na2S2O4 . Na2S2O4俗称保险粉,广泛应用于染料、印染、造纸、食品工业以及医学上.这种技术是最初的电化学脱硫技术之一.请写出该电解反应中阴极的电极方程式:
(4)SO2经过净化后与空气混合进行催化氧化后制取硫酸或者硫酸铵,其中SO2发生催化氧化的反应为:2SO2(g)+O2(g)2SO3(g).若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示:
①该反应的化学平衡常数表达式:K=
②图中A点时,SO2的转化率为
③计算SO2催化氧化反应在图中B点的压强平衡常数K=(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
④若在T2℃,其他条件不变的情况下测得压强的变化曲线如图所示,则T1T2(填“>”、“<”、“=”);其中C点的正反应速率vc(正)与A点的逆反应速率vA(逆)的大小关系为vc(正)vA逆) (填“>”、“<”、“=”).
【答案】
(1)2C3H6+18NO=6CO2+6H2O+9N2
(2)﹣746.5
(3)2HSO3﹣+2H++2e﹣=S2O42﹣+2H2O
(4)![]() ;45%;24300 (Mpa)﹣1;<;>
;45%;24300 (Mpa)﹣1;<;>
【解析】(1)C3H6催化还原尾气中的NO气体,可以得到无毒的气体氮气和二氧化碳,即2C3H6+18NO=6CO2+6H2O+9N2;所以答案是:2C3H6+18NO=6CO2+6H2O+9N2;(2))②×2+③×2﹣①得到2NO(g)+2CO(g)N2(g)+2CO2(g),反应的焓变=2(+110.5kJmol﹣1)+2(﹣393.5kJmol﹣1)﹣(180.5kJmol﹣1)=﹣746.5kJmol﹣1 , 所以答案是:﹣746.5kJmol﹣1;(3)电解反应中阴极上发生得电子的还原反应,2HSO3﹣+2H++2e﹣=S2O42﹣+2H2O,所以答案是:2HSO3﹣+2H++2e﹣=S2O42﹣+2H2O;(4)①2SO2(g)+O2(g)2SO3 , 反应的平衡常数K= 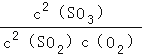 ,所以答案是:
,所以答案是: 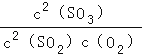 ;
;
②依据化学三行列式计算,设氧气消耗物质的量为x,
2SO2(g)+O2(g)2SO3
起始量(mol) 2a a 0
变化量(mol) 2x x 2x
平衡量(mol)2a﹣2x a﹣x 2x
图中A点时,气体物质的量0.085,则 ![]() =
= ![]() ,x=0.45aSO2的转化率=
,x=0.45aSO2的转化率= ![]() ×100%=45%,
×100%=45%,
所以答案是:45%;
③图中B点,依据化学三行列式计算,设氧气消耗物质的量为y,
2SO2(g)+O2(g)2SO3
起始量(mol) 2a a 0
变化量(mol) 2y y 2y
平衡量(mol)2a﹣2y a﹣y 2y
B点气体物质的量为 0.007,则 ![]() =
= ![]() ,y=0.9a,平衡常数K=(
,y=0.9a,平衡常数K=( 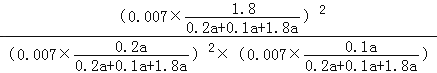 )=24300(MPa)﹣1 ,
)=24300(MPa)﹣1 ,
所以答案是:24300(MPa)﹣1;
④图象分析可知,先拐先平温度高则T1<T2 , C点是平衡状态,A点反应未达到平衡状态,其中C点的正反应速率vC(正)与A点的逆反应速率vA(逆)的大小关系为vC(正)>vA(逆)
所以答案是:<,>.
【考点精析】本题主要考查了反应热和焓变和反应速率的定量表示方法的相关知识点,需要掌握在化学反应中放出或吸收的热量,通常叫反应热;反应速率的单位:mol/(L·min)或mol/(L·s) v=△c-△t才能正确解答此题.

 阅读快车系列答案
阅读快车系列答案【题目】如表是元素周期表的一部分,用化学用语回答:
族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
二 | ] | ① | ② | ||||
三 | ③ | ④ | ⑤ | ⑥ | |||
四 | ⑦ |
(1)②的元素符号为 .
(2)比较元素③和⑦的原子半径大小:③⑦(填“>”或“<”).
(3)绘出元素⑤的离子结构示意图 .
(4)元素①的氢化物的电子式为 , 将该氢化物通入④和⑥形成的化合物的水溶液中,发生反应的离子方程式为 .