题目内容
5.实验室中利用下图所示装置制备纳米碳酸钙(1纳米=1×10-9m)(部分夹持装置已略去),向饱和CaCl2溶液中通入NH3和CO2可制得纳米碳酸钙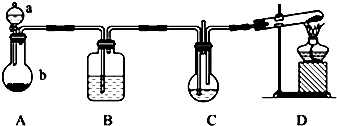
供选择的药品:①石灰石 ②氯化铵 ③氢氧化钙 ④饱和氯化钙溶液 ⑤浓硫酸
⑥6mol•L-1盐酸 ⑦饱和食盐水 ⑧饱和NaHCO3溶液
(1)装置A中,仪器a的名称是分液漏斗,仪器b中应盛放的固体为①.(填药品序号).装置B中盛放的溶液是⑧(填药品序号).装置D的试管中发生反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$aCl2+2NH3↑+2H2O.
(2)如何判断所得碳酸钙颗粒是否为纳米级.将少量碳酸钙加水充分搅拌,用一束可见光照射,观察是否发生丁达尔现象,若有丁达尔现象则为纳米级,若没有丁达尔现象则不是纳米级.
(3)通入适量气体后,C装置中物质恰好完全反应,过滤,所得滤液显酸(填“酸”、“碱”、“中”之一)性.
(4)装置C中,右边的导管并未插入液面,原因是防止装置C的溶液倒吸到装置D中引起试管爆裂
(5)上述装置存在一处缺陷,该缺陷为无尾气吸收装置.
分析 (1)根据装置特点可知A为石灰石与盐酸反应制二氧化碳的发生装置,E为氨气的发生装置;由A制得的二氧化碳中含有氯化氢气体,装置B目的是除掉挥发出来的氯化氢;实验室制取氨气采用氯化铵和氢氧化钙加热制的生成氯化钙、氨气和水;
(2)将少量碳酸钙加水充分搅拌,看是否有丁达尔效应;
(3)C装置中是向饱和CaCl2溶液中通入NH3和CO2,反应生成碳酸钙和氯化铵,恰好完全反应后,过滤,所得滤液为氯化铵溶液,铵根在水中发生水解;
(4)氨气极易溶于水,容易发生倒吸;
(5)根据装置图可知,反应结束后C装置中导管直接与空气相通,没有尾气处理,会污染空气;
解答 解:(1)仪器a的名称是分液漏斗;仪器b中为碳酸钙与盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑,所以仪器b中应盛放的固体为石灰石,故选①,装置B中盛放的饱和NaHCO3溶液可除掉挥发出来的氯化氢,故选⑧,装置D中制取氨气,化学方程式为2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$aCl2+2NH3↑+2H2O,
故答案为:分液漏斗;①;⑧;2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$aCl2+2NH3↑+2H2O;
(2)将少量碳酸钙加水充分搅拌,看是否有丁达尔效应,若有丁达尔效应,则说明为纳米级,
故答案为:将少量碳酸钙加水充分搅拌,用一束可见光照射,观察是否发生丁达尔现象,若有丁达尔现象则为纳米级,若没有丁达尔现象则不是纳米级;
(3)C装置中发生反应CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl,铵根在水中发生水解显酸性,
故答案为:酸;
(4)氨气极易溶于水,容易发生倒吸,所以装置C中,右边的导管并未插入液面是防止装置C的溶液倒吸到装置D中引起试管爆裂,
故答案为:防止装置C的溶液倒吸到装置D中引起试管爆裂;
(5)根据装置图可知,反应结束后C装置中导管直接与空气相通,没有尾气处理,会污染空气,所以装置存在一处缺陷为无尾气吸收装置,
故答案为:无尾气吸收装置.
点评 本题考查化学实验、离子方程式的书写等,难度中等,涉及常见气体的制备等知识,注意纳米材料可用丁达尔效应判断.

 考前必练系列答案
考前必练系列答案| A. | 1:2:3 | B. | 3:2:1 | C. | 1:1:1 | D. | 无法计算 |
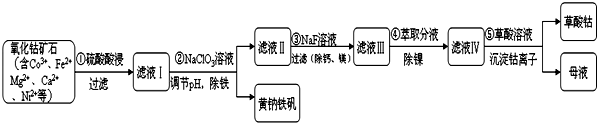
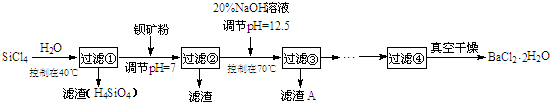
(1)步骤①中研究矿石粒度对钴浸出率的影响如表.从表中分析选择矿石粒度为-200目.
| 序号 | 矿石粒度/目 | 钴浸出率/% |
| 1 | -60 | 9.8 |
| 2 | -120 | 25.5 |
| 3 | -200 | 41.18 |
(3)Ⅰ.步骤②中NaClO3将Fe2+氧化成Fe3+的离子方程式并标出电子转移方向和数目
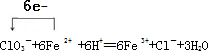 .
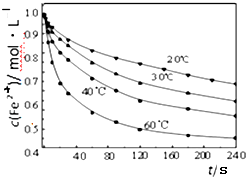
.Ⅱ.探究温度对步骤②中NaClO3将Fe2+氧化成Fe3+的影响,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(Fe2+)的变化,结果如图,请从图中分析最合适的温度下,在0s 至120s内的平均反应速率v(Fe2+)=0.25 mol•L-1•min-1.
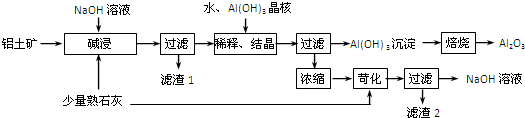
(4)请写出步骤 ③中除去镁离子的离子反应方程式Mg2++2F-=MgF2↓.
(5)若要检验黄钠铁矾[Na2 Fe6(SO4)4(OH)12]中含有的金属元素,请简述实验方案:取黄钠铁矾用盐酸溶液溶解,分成两份,一份做火焰色反应,火焰为黄色证明有Na+存在;另一份向其中滴加KSCN溶液,溶液变成血红色,证明有Fe3+存在.
(6)从绿色化学角度分析,母液中可循环利用的物质为硫酸(填写名称).
 能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO(g)+2H2(g)?CH3OH(g)△H1
反应II:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
①上述反应符合“原子经济”原则的是Ⅰ(填“I”或“Ⅱ”).
②下表所列数据是反应I在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
③某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CH3OH)=0.8mol/L,则CO的转化率为80%,此时的温度为250℃(从上表中选择).
④恒温、恒容时,下列情况不能说明反应I已经达到化学平衡状态的是d.
a、容器各物质的浓度保持不变; b、容器内压强保持不变;
c、υ(CO)消耗═1/2υ(H2)生成 d、容器内的密度保持不变
(2)25℃、101kPa时,燃烧16g液体甲醇生成CO2和H2O(l),放出的热量为363.26kJ,写出甲醇燃烧的热化学方程式:CH3OH(l)+$\frac{3}{2}$O2(g )═CO2(g )+2H2O(l)△H1=-726.52 kJ/mol.
(3)某实验小组依据甲醇燃烧的反应原理,设计一个燃料电池电解Na2SO4溶液(图如下).请根据图示回答下列问题:
①通入甲醇蒸气的电极应为负极(填写“正”或“负”),该电极上发生的电极反应是b(填字母代号).
a.2CH3OH-12e-+3O2═2CO2+4H2O
b.CH3 OH-6e-+8OH-═CO32-+6H2O
c.O2+2H2O+4e-═4OH-
d.O2-4e-+4H+═2H2O
②写出电极A的名称阴极.写出B电极的电极反应式4OH--4e-═O2↑+2H2O.
③当碱性甲醇燃料电池消耗3.36L 氧气时(折合为标准状况),理论上电解Na2SO4溶液生成气体的总物质的量是0.45mol.

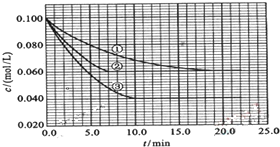 浓度为0.06mol/L.
浓度为0.06mol/L.