题目内容
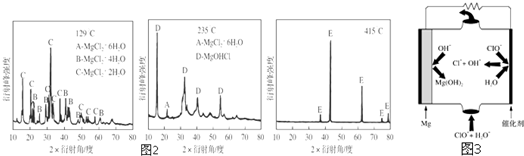
20.高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.高铁酸钾为暗红色粉末状晶体,干燥的晶体80℃以下十分稳定,它极易溶于水,难溶于异丙醇.实验室模拟生产工艺流程如图1:
已知:①2KOH+Cl2=KCl+KClO+H2O(条件:较低温度)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:较高温度)
③K2FeO4 在水溶液中易水解:4FeO42-+10H2O?4Fe(OH)3(胶体)+8OH-+3O2↑
回答下列问题:
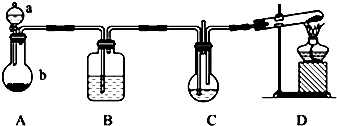
实验室可利用如图2装置完成流程①和②
(1)仪器a的名称是三颈烧瓶,恒压滴液漏斗支管的作用是平衡压强,两水槽中的水为冷水(填“热水”或“冷水”).
(2)反应一段时间后,停止通氯气,再往仪器a中加入浓KOH溶液的目的是与过量的Cl2继续反应,生成更多的KClO;判断浓KOH溶液已过量的实验依据是三颈烧瓶内颜色彻底变成无色后,再加适量的浓氢氧化钾.
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子方程式为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
(4)用重结晶法提纯粗产品:将粗产品先用KOH稀溶液溶解,再加入饱和的KOH溶液,冷却结晶,过滤,用少量异丙醇洗涤,最后低温真空干燥.
①粗产品用KOH溶解的目的是增大氢氧根离子的浓度,抑制FeO42-的水解.
②如何判断K2FeO4晶体已经洗涤干净用试管取少量最后一次的洗涤液,加入硝酸酸化的硝酸银溶液,若无白色沉淀则已被洗净.
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图3.电解过程中阳极的电极反应式为Fe+8OH--6e-═FeO42-+4H2O.
分析 足量Cl2通入和KOH溶液中,温度低时发生反应Cl2+2OH-=Cl-+ClO-+H2O,向溶液I中加入KOH,使氯气完全反应,且将溶液转化为碱性溶液,只有碱性条件下次氯酸根离子才能和铁离子发生氧化还原反应生成高铁酸根离子,除去KCl得到碱性的KClO浓溶液,向碱性的KClO浓溶液中加入90%的Fe(NO3)3溶液,发生反应2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,得到溶液II,纯化得到湿产品,将湿产品洗涤、干燥得到晶体K2FeO4.
(1)根据常用仪器的名称和用途解答;恒压滴液漏斗漏斗支管可以平衡内外压强,使液体顺利滴下;足量Cl2通入和KOH溶液中,温度低时发生反应生成次氯酸根离子;
(2)KOH和氯气在低温下反应生成KClO,只有碱性条件下,铁离子才能和次氯酸根离子发生氧化还原反应生成高铁酸根离子,再往仪器a中加入浓KOH溶液的目的是与过量的Cl2继续反应,生成更多的KClO,氯气为黄绿色气体,判断浓KOH溶液已过量三颈烧瓶内颜色彻底变成无色后,再加适量的浓氢氧化钾;
(3)根据题目信息、氧化还原反应中化合价发生变化确定产物以及电子得失守恒和质量守恒来配平;
(4)①加入饱和KOH溶液可以增大氢氧根离子的浓度,使平衡向左移动;
②只要检验最后一次的洗涤中无Cl-,即可证明K2FeO4晶体已经洗涤干净;
(5)用电解法制备铁酸钠,电解时铁失去电子发生氧化反应结合氢氧根离子生成铁酸跟离子和水.
解答 解:(1)仪器a属于烧瓶,具有三个口,名称是三颈烧瓶,恒压滴液漏斗上部和三颈烧瓶气压相通,可以保证恒压滴液漏斗中的液体顺利滴下,2KOH+Cl2=KCl+KClO+H2O(条件:较低温度),所以两水槽中的水为冷水,
故答案为:三颈烧瓶;平衡压强;冷水;
(2)只有碱性条件下,铁离子才能和次氯酸根离子发生氧化还原反应生成高铁酸根离子,KOH和氯气反应生成KClO,所以加入KOH的目的是除去氯气且使溶液为后一步反应提供碱性,氯气为黄绿色气体,判断浓KOH溶液已过量三颈烧瓶内颜色彻底变成无色后,再加适量的浓氢氧化钾,
故答案为:与过量的Cl2继续反应,生成更多的KClO;三颈烧瓶内颜色彻底变成无色后,再加适量的浓氢氧化钾;
(3)据题目信息和氧化还原反应中化合价发生变化确定找出反应物:Fe3+、ClO-,生成物:FeO42-、Cl-,根据电子得失守恒和质量守恒来配平,Fe3+、ClO-,生成物:FeO42-、Cl-,根据电子得失守恒:Fe(+3→+6),Cl(+1→-1),最小公倍数为6,所以Fe3+、FeO42-前系数都为2,ClO-、Cl-,前系数都为3,结合质量守恒和电荷守恒可得2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
(4)①K2FeO4 在水溶液中易水解:4FeO42-+10H2O?4Fe(OH)3(胶体)+8OH-+3O2↑,加入饱和KOH溶液可以增大氢氧根离子的浓度,使平衡向左移动,抑制FeO42-的水解,
故答案为:增大氢氧根离子的浓度,抑制FeO42-的水解;
②K2FeO4晶体表面若含有杂质离子为氯离子,所以只要检验最后一次的洗涤中无Cl-,即可证明晶体已经洗涤干净,
故答案为:用试管取少量最后一次的洗涤液,加入硝酸酸化的硝酸银溶液,若无白色沉淀则已被洗净;
(5)用铁做阳极电解氢氧化钠制备铁酸钠,电解时铁失去电子发生氧化反应结合氢氧根离子生成铁酸跟离子和水,电极反应式为:Fe+8OH--6e-=FeO42-+4H2O,
故答案为:Fe+8OH--6e-═FeO42-+4H2O.
点评 本题结合高铁酸钾(K2FeO4)的制备主要考查了氧化还原反应的知识、离子的检验等,侧重考查学生分析能力、知识迁移运用能力,题目难度中等.培养了学生运用知识的能力.

 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2 (g)、CO2 (g)和H2O(1)的热化学方程式CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=-955kJ•mol-1.
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理.已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+═4Fe3++2H2O,则另一反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
(3)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g).某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
②根据表中数据,计算T1℃时该反应的平衡常数为0.56(保留两位小数).
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率不变(填“增大”、“不变”或“减小”).
④下列各项能作为判断该反应达到平衡的是CD(填序号字母).
A.容器内压强保持不变 B. 2v正(NO)=v逆(N2)
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
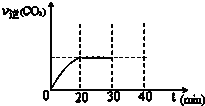
⑤30min末改变某一条件,过一段时间反应重新达到平衡,则改变的条件可能是减小CO2 的浓度.请在图中画出30min至40min的变化曲线.
(1)氯水久置后会变质,请分析变质的原因.(请用方程式及必要文字说明分析)氯气与水反应:H2O+Cl2?HCl+HClO,HClO不稳定分解:2HClO═2HCl+O2↑
(2)如果增大氯气的压强,氯气在水中的溶解度将增大(填“增大”“减小”或“不变”)
Ⅱ、在2L恒容的密闭容器中,加入4mol SO3(g),在某温度下使其反应,反应至4min时,氧气的浓度为0.5mol/L,当反应到8min时,反应到达平衡.
(1)0min~4min内生成O2的平均速率:v(O2)=0.125mol/(L•min).
(2)若8分钟达到平衡时,测得SO3浓度为0.04mol/L.若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于0.04mol/L的是BD
| A | B | C | D | |
| SO3 | 0mol | 4mol | 2mol | 0mol |
| SO2 | 4mol | 1.5mol | 0mol | 4mol |
| O2 | 2mol | 0mol | 0mol | 4mol |
| A. | 氯气通入水中:Cl2+H2O?2H++Cl-+ClO- | |
| B. | KI溶液与H2SO4酸化的H2O2溶液混合:2 I-+H2O2+2 H+=2 H2O+I2 | |
| C. | 向NH4HCO3溶液中滴加过量Ba(OH)2溶液:HCO3-+OH-+Ba2+=H2O+BaCO3↓ | |
| D. | 高锰酸钾酸性溶液吸收二氧化硫:SO2+MnO4-+4H+=SO42-+Mn2++2H2O |
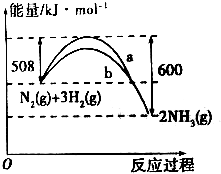 N2与H2反应生成NH3的过程中能量变化曲线如图所示.若在一个固定容积的密闭容器中充入1mol N2和3mol H2使反应N2(g)+3H2(g)?2NH3(g)达到平衡,测得反应放出热量为Q1kJ.
N2与H2反应生成NH3的过程中能量变化曲线如图所示.若在一个固定容积的密闭容器中充入1mol N2和3mol H2使反应N2(g)+3H2(g)?2NH3(g)达到平衡,测得反应放出热量为Q1kJ.