题目内容
【题目】草酸亚铁晶体(FeC2O4·2H2O)是一种黄色难溶于水的固体,受热易分解,是生产锂电池、涂料、着色剂以及感光材料的原材料。
 。
。
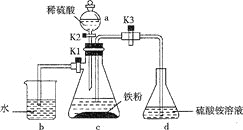
I、制备草酸亚铁晶体:
①称取硫酸亚铁铵晶体5g,放入250mL三颈烧瓶中,加入10滴左右1.0mol·L-1H2SO4溶液和15mL蒸馏水加热溶解;
②加入25mL饱和草酸溶液,加热搅拌至沸,停止加热,静置;
③待黄色晶体FeC2O4·2H2O沉淀后倾析,洗涤,加入约20mL蒸馏水搅拌并温热5min,静置,弃去上层清液,即得黄色草酸亚铁晶体。
回答下列问题:
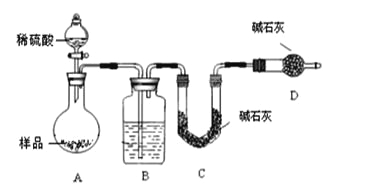
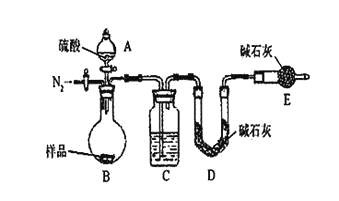
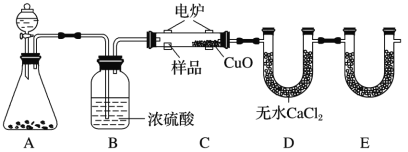
(1)仪器B的作用是___;
(2)硫酸亚铁铵晶体用硫酸溶解的原因是___;
(3)硫酸亚铁铵晶体可能混有一定Fe3+,羟胺(NH2OH,酸性条件下以NH3OH+形式存在)具有强还原性,在酸性条件下可用羟胺去除亚铁盐中的Fe3+。写出相关的离子方程式:__;
II、探究草酸亚铁的纯度:
①准确称取mg草酸亚铁固体样品(含有草酸铵杂质),溶于25mL2mol·L-1H2SO4溶液中,在60~80℃水浴加热,用100mL容量瓶配成100.00mL溶液;
②用___滴定管(填“酸式”、“碱式”)取上述溶液20.00mL,用KMnO4标准溶液(浓度为cmol·L-1)滴定三次,平均消耗V1mL;
③在②反应后的溶液中加入适量锌粉和2mL2 mol·L-1H2SO4溶液,反应一段时间后,取1滴试液放在点滴板上检验,至Fe3+极微量;
④过滤除去锌粉,滤液收集在另一个锥形瓶中,将滤纸及残余物充分洗涤,洗涤液并入滤液中,再补充约2~3mL2mol·L-1 H2SO4溶液,继续用KMnO4标准溶液(浓度为cmol·L-1)滴定至终点,共平行测定三次,平均消耗V2mL。
回答下列问题:
(4)在②中溶液中发生反应MnO4-+8H++5Fe2+=5Fe3++Mn2++4H2O,还有另一氧化还原反应,写出其离子方程式__。
(5)加入适量锌粉的目的是___;步骤③中检验其中微量的Fe3+的试剂是__(用化学式表示)溶液。步骤④用KMnO4标准溶液滴定至终点的现象是___。
(6)计算mg固体样品的纯度为__(用含c、V2的式子表示,不必化简)。
【答案】冷凝回流 抑制Fe2+的水解 2NH3OH++2Fe3+=2Fe2++N2↑+2H2O+4H+ 酸式 2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O 将Fe3+还原为Fe2+ KSCN 最后1滴标准溶液加入后,锥形瓶中的溶液颜色由浅绿色变为浅紫红色,且半分钟内不褪色 ![]() ×100%
×100%
【解析】
I、(1)B为冷凝管,作用即冷凝回流;
(2)硫酸可抑制Fe2+的水解;
(3)羟胺可将Fe3+还原为Fe2+;
II、②样品溶液有酸性,用酸式滴定管量取;
(4)另一反应为高锰酸钾将草酸氧化为CO2的反应;
(5)锌粉可将Fe3+还原为Fe2+,检验Fe3+用KSCN 溶液,出现血红色,滴定至终点时,最后1滴标准溶液加入后,锥形瓶中的溶液颜色由浅绿色变为浅紫红色;
(6)通过方程式导出关系式:KMnO4~5FeC2O4·2H2O,代入数据进行计算。
I、(1)由题意可知,仪器B的作用是冷凝回流;
(2)用硫酸溶解硫酸亚铁铵晶体可抑制Fe2+的水解;
(3)硫酸亚铁铵晶体可能混有一定Fe3+,羟胺(NH2OH,酸性条件下以NH3OH+形式存在)具有强还原性,在酸性条件下可用羟胺去除亚铁盐中的Fe3+,离子方程式为2NH3OH++2Fe3+=2Fe2++N2↑+2H2O+4H+;
II、②草酸亚铁固体样品(含有草酸铵杂质),溶于25mL2mol·L-1H2SO4溶液中配制成样品溶液,所以应用酸式滴定管;
(4)在②中溶液中发生反应MnO4-+8H++5Fe2+=5Fe3++Mn2++4H2O,草酸亚铁和草酸铵和硫酸反应后生成草酸,也能被高锰酸钾溶液氧化,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
(5)加入适量锌粉的目的是将Fe3+还原为Fe2+,步骤③中检验其中微量的Fe3+的试剂是KSCN 溶液,步骤④用KMnO4标准溶液滴定至终点的现象是最后1滴标准溶液加入后,锥形瓶中的溶液颜色由浅绿色变为浅紫红色,且半分钟内不褪色;
(6)由关系式KMnO4 ~ 5 FeC2O4·2H2O
1 5×180
c×V2×10-3 ×![]() m
m
解得m=4.5cV2,所以mg固体样品的纯度为![]() ×100%。
×100%。