题目内容
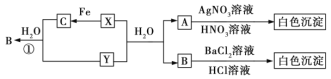
【题目】已知X、Y均为有刺激性气味的气体,且几种物质间有以下转化关系,部分产物未标出。请回答下列问题。
(1)写出下列各物质的化学式:
X______、Y______、A______、B______、C______。
(2)反应①的离子方程式为____________。
【答案】Cl2 SO2 HCl H2SO4 FeCl3 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
【解析】
A与硝酸酸化的AgNO3溶液反应产生白色沉淀,A中含Cl-;B与盐酸酸化的BaCl2溶液反应产生白色沉淀,B中含SO42-;又根据X、Y均为有刺激性气味的气体,且X能与![]() 反应,则X为Cl2,Y为SO2,A为HCl,B为H2SO4,C为FeCl3。
反应,则X为Cl2,Y为SO2,A为HCl,B为H2SO4,C为FeCl3。
(1)分析可知,X为Cl2,Y为SO2,A为HCl,B为H2SO4,C为FeCl3。
(2)反应①为氯化铁与二氧化硫发生氧化还原反应,离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+。

练习册系列答案
相关题目