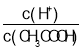��Ŀ����
����Ŀ��ú�������Ǹ�Ч����������ú̿����Ҫ;��֮һ��
��C(s)+O2(g)=CO2(g) ��H=-393.5kJ��mol-1
��CO(g)+![]() O2(g)=CO2(g)��H=-283.0kJ��mol-1
O2(g)=CO2(g)��H=-283.0kJ��mol-1
��H2(g)+![]() O2(g)=H2O(g)��H=-241.8kJ��mol-1
O2(g)=H2O(g)��H=-241.8kJ��mol-1
��1����̼��ˮ������Ӧ����һ����̼���������Ȼ�ѧ����ʽ��_______���÷�Ӧ�Ļ�ѧƽ�ⳣ��K���¶ȵ����߽�_______������������������С����������������
��2��CO������H2O(g)��һ��������ӦCO(g)+H2O(g)![]() CO2(g)+H2(g) ��H��0���ڼס������������ܱ������У���ʼʱ�����±����ݽ���Ͷ�ϣ���800��ʱ�ﵽƽ��״̬��K=1.0��
CO2(g)+H2(g) ��H��0���ڼס������������ܱ������У���ʼʱ�����±����ݽ���Ͷ�ϣ���800��ʱ�ﵽƽ��״̬��K=1.0��
H2O | CO | CO2 | H2 | |
�� n/mol | 0.10 | 0.30 | 0.10 | 0.50 |
�� n/mol | 0.20 | 0.20 | 0 | 0 |
��ʼʱ���������з�Ӧ��____________����������Ӧ�������淴Ӧ����������У�ƽ��ʱ����������CO��ת����Ϊ___________��
���𰸡�C(s��+H2O��g��=CO(g)+H2(g) ��H=+131.3kJ��mol-1 ���� �淴Ӧ 50%
��������
��1�����ݸ�˹���ɣ�����֪�Ȼ�ѧ����ʽ�����ʵ���ϵ�����мӼ�����Ŀ���Ȼ�ѧ����ʽ����Ӧ��Ҳ������Ӧ��ϵ��������Ӧ�ļ��㣬�����¶�ʹƽ���ƶ��Լ�ƽ�ⳣ����ϵ������
��2��������֪Ũ�����Qc��Ȼ����K�Ƚϣ���μӷ�Ӧ��CO�����ʵ���Ϊnmol����������ʽ��ʾ��ƽ��ʱ����ֵ����ʵ��������ڷ�Ӧǰ�������������䣬�������ʵ�������Ũ�ȴ���ƽ�ⳣ���з��̼��㡣
��1����֪����C��s��+O2��g���TCO2��g����H=-393.5kJ/mol
��CO��g��+![]() O2��g���TCO2��g����H=-283.0kJ/mol
O2��g���TCO2��g����H=-283.0kJ/mol
��H2��g��+![]() O2��g���TH2O��g����H=-241.8kJ/mol��
O2��g���TH2O��g����H=-241.8kJ/mol��
���ݸ�˹���ɣ���-��-�ڵ�C��s��+H2O��g��=CO��g��+H2��g����H=+131.3kJmol-1�����ڸ÷�ӦΪ���ȷ�Ӧ�����������¶�ƽ�����ƣ�K����
��2�����������Ϊ1L���������У�Qc=![]() =
=![]() =
=![]() >1=K�����Է�Ӧ���淴Ӧ���У�
>1=K�����Է�Ӧ���淴Ӧ���У�
��μӷ�Ӧ��CO�����ʵ���Ϊnmol����
CO��g��+H2O��g��![]() CO2��g��+H2��g��
CO2��g��+H2��g��
��ʼ��mol���� 0.1 0.1 0 0
ת����mol���� n n n n
ƽ�⣨mol���� 0.1-n 0.1-n n n
��![]() =1�����n=0.05����CO��ת����Ϊ
=1�����n=0.05����CO��ת����Ϊ![]() ��100%=50%��
��100%=50%��

 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�