题目内容
7.溶液的酸碱性对许多物质的氧化性有很大影响;生成物的溶解性会影响复分解反应的方向.将Na2S溶液滴加到FeCl3溶液中,有单质硫生成;将FeC13溶液滴加到Na2S溶液中生成的是Fe2S3而不是S或Fe(OH)3.从以上反应可得出的结论是酸性条件氧化性:Fe3+>S、给出Fe3+能力:Fe(OH)3>Fe2S3.分析 氯化铁为强酸弱碱盐水解显酸性,将Na2S溶液滴加到FeCl3溶液中,有单质硫生成,反应方程式为:2Fe3++S2-═2Fe2++S↓,依据氧化性强弱规律解答;
硫化钠溶液为强碱弱酸盐水解显碱性,将FeC13溶液滴加到Na2S溶液中生成的是Fe2S3,离子方程式为:Fe3++S2-=Fe2S3,依据溶度积规则解答;
解答 解:氯化铁为强酸弱碱盐水解显酸性,将Na2S溶液滴加到FeCl3溶液中,有单质硫生成,反应方程式为:2Fe3++S2-═2Fe2++S↓,反应中三价铁离子为氧化剂,硫为氧化产物,氧化剂的氧化性大于氧化产物的氧化性,所以
酸性条件氧化性:Fe3+>S;
硫化钠溶液为强碱弱酸盐水解显碱性,将FeC13溶液滴加到Na2S溶液中生成的是Fe2S3,离子方程式为:Fe3++S2-=Fe2S3,说明硫化铁溶解度小于氢氧化铁,给出Fe3+能力:Fe(OH)3>Fe2S3;
故答案为:酸性条件氧化性:Fe3+>S;给出Fe3+能力:Fe(OH)3>Fe2S3;
点评 本题考查了氧化还原反应规律、溶度积规则,明确相关知识是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.“优先反应思想”是一条重要的化学学科思想.根据所学知识及题目提供的相关数据,回答下列问题:
(1)向FeBr2溶液中滴加少量氯水,溶液变黄.你认为使溶液变黄的微粒其符号是Fe3+,用实验证明你的观点,简述实验操作及现象取适量反应后的溶液滴加KSCN溶液变红.
(2)用惰性电极电解由等物质的量的NaBr、KI、NaCl组成的混合溶液,阳极首先发生的电极反应式是2I--2e-=I2.
(3)已知常温下一些电解质的相关数据如表:
①向等物质的量浓度的Na2CO3、CH3COONa、NaClO组成的混合溶液中逐滴加入稀硫酸,首先发生反应的离子方程式是CO32-+H+=HCO3-.
②向浓度均为0.010mol•L-1的NaCl、Na2CrO4组成的混合溶液中逐滴加入浓度为0.010mol•L-1AgNO3溶液,首先生成的沉淀其化学式为AgCl.
(4)分别向四份各100mL、浓度均为2mol•L-1的FeCl3溶液中,加入铁、铜组成的均匀粉末状混合物,得到如下数据:
①根据表中的数据可求出粉末中铁、铜的物质的量之比为1:1.
②根据表中的数据分析Ⅰ反应后的溶液中存在的金属阳离子有(用离子符号表示)Fe3+、Fe2+、Cu2+.
(1)向FeBr2溶液中滴加少量氯水,溶液变黄.你认为使溶液变黄的微粒其符号是Fe3+,用实验证明你的观点,简述实验操作及现象取适量反应后的溶液滴加KSCN溶液变红.
(2)用惰性电极电解由等物质的量的NaBr、KI、NaCl组成的混合溶液,阳极首先发生的电极反应式是2I--2e-=I2.
(3)已知常温下一些电解质的相关数据如表:
| H2CO3 | Ka1=4.3×10-7 | HClO | Ka=2.95×10-8 |
| Ka2=5.61×10-11 | AgCl | Ksp=1.77×10-10 | |
| CH3COOH | Ka=1.76×10-5 | Ag2CrO4 | Ksp=1.12×10-12 |
②向浓度均为0.010mol•L-1的NaCl、Na2CrO4组成的混合溶液中逐滴加入浓度为0.010mol•L-1AgNO3溶液,首先生成的沉淀其化学式为AgCl.
(4)分别向四份各100mL、浓度均为2mol•L-1的FeCl3溶液中,加入铁、铜组成的均匀粉末状混合物,得到如下数据:
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | |
| FeCl3溶液体积/mL | 100 | 100 | 100 | 100 |
| 加入粉末质量/g | 3 | 6.6 | 9 | 12 |
| 剩余粉末质量/g | 0 | 0.64 | 3.2 | 6.4 |
②根据表中的数据分析Ⅰ反应后的溶液中存在的金属阳离子有(用离子符号表示)Fe3+、Fe2+、Cu2+.
18.下列说法正确的是( )
| A. | 青铜、碳素钢和石英都是合金 | |
| B. | 陶瓷、玻璃和水泥都是无机非金属材料 | |
| C. | 乙醇与乙醛互为同分异构体,都能发生银镜反应 | |
| D. | 油脂皂化和蛋白质水解都是由高分子生成小分子的过程 |
15.下列关于化学反应速率的说法中正确的是( )
| A. | 化学反应速率可用某时刻生成物的物质的量来表示 | |
| B. | 在同一反应中,用反应物或生成物表示的化学反应速率的值是相对的 | |
| C. | 化学反应速率是指反应进行的时间内,反应物浓度的减少或生成物浓度的增加 | |
| D. | 可用单位时间内氢离子物质的量浓度的变化来表示氢氧化钠和硫酸的反应速率 |
2.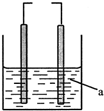 如图的装置,左为铁电极,右为石墨电极,a为水或某种溶液.若两电极直接连接或外接电源,石墨上可能发生的反应是( )
如图的装置,左为铁电极,右为石墨电极,a为水或某种溶液.若两电极直接连接或外接电源,石墨上可能发生的反应是( )
①2H++2e→H2↑ ②O2+4e+2H2O→4OH- ③2Cl--2e→Cl2↑
 如图的装置,左为铁电极,右为石墨电极,a为水或某种溶液.若两电极直接连接或外接电源,石墨上可能发生的反应是( )
如图的装置,左为铁电极,右为石墨电极,a为水或某种溶液.若两电极直接连接或外接电源,石墨上可能发生的反应是( )①2H++2e→H2↑ ②O2+4e+2H2O→4OH- ③2Cl--2e→Cl2↑
| A. | ① | B. | ② | C. | ①② | D. | ①②③ |
12.下列化学用语使用正确是( )
| A. | 氧原子能量最高的电子的电子云图: | |
| B. | 35Cl与37Cl互为同素异形体 | |
| C. | CH4分子的比例模型: | |
| D. | 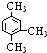 的命名:1,3,4-三甲苯 的命名:1,3,4-三甲苯 |
19.向等物质的量浓度的NaOH和Ca(OH)2的混合液中通入一定量CO2.下列离子方程式与事实不相符的是( )
| A. | OH-+CO2→HCO3- | |
| B. | 2OH-+CO2→CO32-+H2O | |
| C. | Ca2++2OH-+CO2→CaCO3↓+H2O | |
| D. | Ca2++4OH-+2CO2→CaCO3↓+CO32-+2H2O |
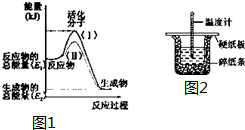 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ•mol-1表示.请认真观察如图1,然后回答问题.
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ•mol-1表示.请认真观察如图1,然后回答问题.