题目内容
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.往沸水中滴加0.1molFeCl3饱和溶液,制得的胶体中含0.1NA个Fe(OH)3胶体粒 |
| B.标准状况下,11.2L C2H6含3NA个C—H极性共价键 |
| C.标准状况下,5.6 L NO和5.6 L O2混合后的分子总数为0.5 NA |
| D.标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA |
B
解析试题分析:A、铁离子水解是可逆反应,所以往沸水中滴加0.1molFeCl3饱和溶液,制得的胶体中Fe(OH)3胶体粒的个数小于0.1NA个,A不正确;B、标准状况下,11.2L乙烷的物质的量是0.5mol,含0.5×6=3NA个C—H极性共价键,B正确;C、NO和氧气混合后发生反应2NO+O2=2NO2,所以标准状况下,5.6 L NO和5.6 L O2混合后的分子总数小于0.5 NA,C不正确;D、标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为2NA,D不正确,答案选B。
考点:考查阿伏加德罗常数的有关计算

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.3mol NF3与水完全反应生成HNO3和NO,转移电子数2NA |
| B.4.4g14CO2含中子数2.4 NA |
| C.标准状况下,2.24L Cl2通入足量NaOH溶液中,反应转移电子的数目为0.2NA |
| D.常温常压下,1.7g H2O2中含有的电子数为NA |
将Cu片放入0.1mol·L-1 FeCl3溶液中,反应进行一定时间后,取出Cu片,测得溶液中c(Fe3+)︰c(Fe2+)=2︰3,则此时溶液中Cu2+与Fe3+的物质的量之比为
| A.3︰2 | B.3︰5 | C.3︰4 | D.4︰3 |
将35.8g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生6.72L气体(标准状况)。另取等质量的该合金溶于过量的稀硝酸中,生成13.44L NO(标准状况),向反应后的溶液中加入足量的NaOH溶液,得到沉淀的质量为
| A.66.4 g | B.50.8 g | C.44.8g | D.39.2g |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.0.1mol的2H35Cl含中子数为1.8NA |
| B.16g O3和O2混合物中氧原子数为NA |
| C.常温下,1L pH=l的溶液中H+的数目大于0.1NA |
| D.0.1 mol的H2O2中含有非极性键数为0.2NA |
用NA表示阿伏伽徳罗常数的值,下列说法正确的是( )
| A.常温常压下,26g乙炔含有的∏键数目为3NA |
| B.7.8gNa2O2中所含阴离子的数目是0.2NA |
| C.标准状况下,2.24Ll8O2中所含中子的数目是2NA |
| D.在密闭容器中盛有0.lmolN2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6 NA |
一定质量的某铁的氧化物FexOy,与足量4 mol/L稀硝酸溶液充分反应,消耗硝酸700mL,放出2.24LNO气体(标准状况)。则该铁的氧化物的化学式为
| A.FeO | B.Fe2O3 | C.Fe3O4 | D.Fe8O10 |
若NA表示阿伏加德罗常数的值,下列说法正确的是
| A.铁制品上电镀锌时,阴极质量每增加65g时转移的电子数是2NA |
| B.5.6L Cl2与足量铁粉反应时转移的电子数为0.5NA |
| C.1L 1mol·L-1的CH3COOH溶液中含有H+的数目是NA |
| D.1L 0.5mol·L-1的Na2CO3溶液中含有CO32-的数目是0.5NA |
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。 据此下列说法错误的是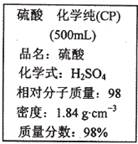
| A.该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管 |
| B.取10 mL该硫酸于烧杯中,再加等体积的水,可配得49%的硫酸 |
| C.配制200mL4.6 mol·L-1的稀硫酸需取该硫酸50 mL |
| D.该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2 mol·L-1 |