题目内容
若NA表示阿伏加德罗常数的值,下列说法正确的是
| A.铁制品上电镀锌时,阴极质量每增加65g时转移的电子数是2NA |
| B.5.6L Cl2与足量铁粉反应时转移的电子数为0.5NA |
| C.1L 1mol·L-1的CH3COOH溶液中含有H+的数目是NA |
| D.1L 0.5mol·L-1的Na2CO3溶液中含有CO32-的数目是0.5NA |
A
解析试题分析:A.阴极质量每增加65g时生成1mol锌,转移的电子数是2NA,正确;B.没有说明是否为标准状况下,错误;C.CH3COOH是弱酸,不能完全电离,溶液中含有H+的数目小于NA,错误;D.CO32-水解,数目小于0.5NA,错误。
考点:阿伏加德罗常数

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
下列叙述正确的是
| A.3.01×1023个SO2分子的质量为32g |
| B.CH4的摩尔质量为16g |
| C.1 mol H2O的质量为18g/mol |
| D.标准状况下,1 mol任何物质体积均为22.4L |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.往沸水中滴加0.1molFeCl3饱和溶液,制得的胶体中含0.1NA个Fe(OH)3胶体粒 |
| B.标准状况下,11.2L C2H6含3NA个C—H极性共价键 |
| C.标准状况下,5.6 L NO和5.6 L O2混合后的分子总数为0.5 NA |
| D.标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.等物质的量的N2和CO所含分子数均为NA |
| B.标准状况下,11.2 L氟化氢所含的分子数为0.5NA |
| C.常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.5NA |
| D.常温常压下,14.9g KCl与NaClO的混合物中含氯元素的质量为7.1g |
对相同状况下的12C18O和14N2两种气体,下列说法正确的是
| A.若质量相等,则质子数相等 |
| B.若原子数相等,则中子数相等 |
| C.若分子数相等,则体积相等 |
| D.若体积相等,则密度相等 |
下列有关化学用语使用正确的是
A.CH4分子的球棍模型: |
| B.乙烯的结构简式:CH2CH2 |
C.S的结构示意图: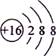 |
D.原子核内有l8个中子的氯原子: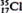 |
下列叙述中正确的是
| A.相同条件下,N2和O3的混合气体与等体积的N2所含原子数相等 |
| B.标准状况下,28g CO与22.4LSO3所含分子数相等 |
| C.5.6g铁粉与足量氯气充分反应,有0.2mol电子转移 |
| D.等物质的量的CH5+和NH2-所含电子数相等 |
有4.8g CuO、Fe2O3混合物跟足量CO充分反应后固体减少1.28g,反应后全部气体用0.6mol/L Ba(OH)2溶液100mL吸收。下列有关叙述中正确的是
| A.原混合物中CuO与Fe2O3物质的量的比为l:l |
| B.原混合物中CuO与Fe2O3的质量比为2:1 |
| C.吸收CO2后的溶液中一定有Ba(HCO3)2 |
| D.吸收CO2后的溶液中生成白色沉淀的质量为11.82 g |
化学科学需要借助化学专用语言来描述。下列有关化学用语表示正确的是
A.丙烷的球棍模型: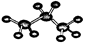 |
B.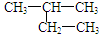 的名称:2-乙基丙烷 的名称:2-乙基丙烷 |
| C.乙酸的分子式:CH3COOH |
| D.氧化钠的化学式:Na2O2 |