题目内容
【题目】元素铬(Cr)在自然界主要以+3价和+6价存在。请回答下列问题:
(1)+6价的Cr能引起细胞的突变而对人体不利,可用 Na2SO3 将Cr2O72—还原为Cr3+。该反应的离子反应方程式为___________。
(2)利用铬铁矿(FeOCr2O3)冶炼制取金属铬的工艺流程如图所示:

①为加快焙烧速率和提高原料的利用率,可采取的措施之一是__________________________ 。
②“水浸”要获得浸出液的操作是_________________________________。浸出液的主要成分为Na2CrO4,向“滤液”中加入酸化的氯化钡溶液有白色沉淀生成,则 “还原”操作中发生反应的离子方程式为___。
③加热Cr(OH)3可得到Cr2O3,从工业成本角度考虑,用Cr2O3制取金属Cr的冶炼方法是 _______。
(3)已知 Cr3+完全沉淀时溶液pH为5,(Cr3+浓度降至10-5molL-1可认为完全沉淀)则Cr(OH)3的溶度积常数 Ksp=_______________。
(4)用石墨电极电解铬酸钠(Na2CrO4)溶液,可制重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2Cr![]() +2H+
+2H+![]() Cr2
Cr2![]() + H2O)。
+ H2O)。
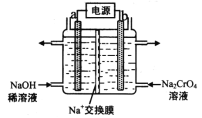
①电极b连接电源的______极(填“正”或“负”) , b 极发生的电极反应式为_________________。
②电解一段时间后,测得阳极区溶液中Na+物质的量由a mol变为b mol,则理论上生成重铬酸钠的物质的量是 _______________mol 。
【答案】Cr2O72—+3SO32-+8H+=2Cr3++3SO42-+4H2O 铬铁矿粉碎 过滤 8CrO42—+3S2-+20H2O=8Cr(OH)3↓+3SO42-+16OH- CO高温还原Cr2O3(热还原法) 1×10-32 正 2H2O-4e-=O2↑+4H+ ![]()
【解析】
(1)分析元素化合价变化情况,依据得失电子守恒,原子个数守恒,得出离子反应方程式。
(2)①影响化学反应速率的因素:物质的表面积大小,表面积越大,反应速率越快。
②依据原子守恒和得失电子守恒,得出离子方程式。
③用Cr2O3制取金属Cr,可以采取CO高温还原Cr2O3(热还原法)。
(3)根据Ksp=c(Cr3+)c3(OH-)求算。
(4)①根据装置图和离子放电顺序得出阳极的电极反应式。
②电解一段时间后,测得阳极区溶液中Na+物质的量由a mol变为b mol,则溶液中移动的电荷为(a-b)mol,所以外电路转移的电子为(a-b)mol,阳极的电极反应为2H2O-4e-=O2↑+4H+,则阳极生成的氢离子为(a-b)mol。
(1)反应中铬元素化合价从+6价降为+3价,硫元素从+4价升高到+6价,依据得失电子守恒,原子个数守恒,离子反应方程式为Cr2O72—+3SO32-+8H+=2Cr3++3SO42-+4H2O,故答案为:Cr2O72—+3SO32-+8H+=2Cr3++3SO42-+4H2O。
(2)①影响化学反应速率的因素:物质的表面积大小,表面积越大,反应速率越快,为加快焙烧速率和提高原料的利用率,可采取的措施将铬铁矿粉碎,故答案为:铬铁矿粉碎。
②“水浸”要获得浸出液,要过滤出浸渣,采取的操作是过滤;浸出液的主要成分为Na2CrO4,向“滤液”中加入酸化的氯化钡溶液有白色沉淀生成,说明加入的Na2S被氧化成SO42-,Cr元素由+6价降为+3价,S元素由-2价升到+6价,依据原子守恒和得失电子守恒,得到反应为:8CrO42—+3S2-+20H2O=8Cr(OH)3↓+3SO42-+16OH-,故答案为:过滤;8CrO42—+3S2-+20H2O=8Cr(OH)3↓+3SO42-+16OH-。
③从工业成本角度考虑,用Cr2O3制取金属Cr,可以采取CO高温还原Cr2O3(热还原法),故答案为:CO高温还原Cr2O3(热还原法)。
(3)pH为5,c(OH-)=10-9,Ksp=c(Cr3+)c3(OH-)=10-5×(10-9)3=1×10-32,故答案为:1×10-32。
(4)①根据图示,在b极所在电极室得到Na2Cr2O7,根据2CrO42-+2H+![]() Cr2O72—+ H2O ,电解过程中b极c(H+)增大,则b极电极反应式为2H2O-4e-=O2↑+4H+,a是阴极,b是阳极,电极b连接电源的正极,故答案为:正;2H2O-4e-=O2↑+4H+。
Cr2O72—+ H2O ,电解过程中b极c(H+)增大,则b极电极反应式为2H2O-4e-=O2↑+4H+,a是阴极,b是阳极,电极b连接电源的正极,故答案为:正;2H2O-4e-=O2↑+4H+。
②电解一段时间后,测得阳极区溶液中Na+物质的量由a mol变为b mol,则溶液中移动的电荷为(a-b)mol,阴极电极反应式为2H2O+2e-=H2↑+2OH-,则电路中通过电子物质的量为(a-b)mol;阳极的电极反应式为2H2O-4e-=O2↑+4H+,则阳极生成的氢离子为(a-b)mol,结合2CrO42-+2H+![]() Cr2O72—+ H2O,所以阳极生成的Cr2O72—物质的量是
Cr2O72—+ H2O,所以阳极生成的Cr2O72—物质的量是![]() mol,故答案为:
mol,故答案为:。

 阅读快车系列答案
阅读快车系列答案【题目】M、N、X、Y四种主族元素在周期表里的相对位置如下图所示,已知它们的原子序数总和为46。

(1)M与Y形成的化合物中含________键,属__________分子。(填“极性”或“非极性”)
(2)N元素形成的单质分子中的化学键类型及数目是__________________(填“σ键”或“π键”)。在化学反应中________易断裂。
(3)由N、Y的氢化物相互作用所生成的物质的电子式为_________________。其中的化学键有__________________________。
(4)写出M单质与X元素最高价氧化物对应的水化物反应的化学方程式_____________。
(5)核电荷数比X元素少8的元素可形成多种粒子,按要求填入空格中:
质子数 | 16 | 16 | 16 |
电子数 | 16 | 17 | 18 |
化学式 | _______ | ________ | ________ |
【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 | H2C2O 4 | K1=5.4×10-2 K2=5.4×10-5 | H2S | K1=1.3×10-7 K2=7.1×10-15 |
HClO | 3×10-8 |
请回答下列问题:
(1)同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是__________。
(2)常温下0.1 molL-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填序号)。
A.c(H+) B. c(H+)/c(CH3COOH) C. c(H+)/c(OH-) D. c(OH-)
(3)0.1 molL-1的H2C2O4溶液与0.1 molL-1的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为______________。
(4)pH相同的NaClO和CH3COOK溶液,其溶液的物质的最浓度的大小关系是:CH3COONa______NaClO,两溶液中:[c(Na+)-c(ClO-)]______[c(K+)-c(CH3COO-)](填“>”“<”或“=”)。
(5)向0.1 molL-1CH3COOH 溶液中滴加 NaOH 溶液至 c(CH3COOH): c(CH3COO-)=5 : 9,此时溶液pH=_______________。