题目内容
【题目】25℃时,几种弱酸的电离平衡常数如下表所示,下列说法正确的是
化学式 | HCOOH | H2CO3 | HCN |
电离平衡常数 | K=1.8×10-4 | K1=4.3×10-7 K2=5.6×10-11 | K=4.9×10-10 |
A. H2CO3溶液和NaCN溶液反应的离子方程式为H2CO3+CN-==HCO3-+HCN
B. HCOOH的电离平衡常数表达式为K= c(HCOOH)/[c(HCOO-)·c(H+)]
C. Na2CO3溶液显碱性,NaHCO3溶液显酸性
D. 酸性强弱顺序是HCOOH>HCN>H2CO3
【答案】A
【解析】A.酸的电离平衡常数HCOOH>H2CO3>HCN>HCO3-,酸性强弱顺序是HCOOH>H2CO3>HCN->HCO3-,H2CO3溶液和NaCN溶液反应的离子方程式为H2CO3+CN-=HCO3-+HCN,故A正确;B.甲酸电离平衡常数K=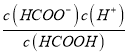 ,故B错误;C.NaHCO3溶液中碳酸氢根离子水解,HCO3-+H2OH2CO3+OH-,水解平衡常数Kh=
,故B错误;C.NaHCO3溶液中碳酸氢根离子水解,HCO3-+H2OH2CO3+OH-,水解平衡常数Kh=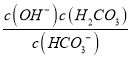 =
=![]() =
=![]() =2.3×10-8>Ka2,水解程度大,溶液显碱性,故C错误;D.酸的电离平衡常数HCOOH>H2CO3>HCN>HCO3-,酸性强弱顺序是HCOOH>H2CO3>HCN,故D错误;故选A。
=2.3×10-8>Ka2,水解程度大,溶液显碱性,故C错误;D.酸的电离平衡常数HCOOH>H2CO3>HCN>HCO3-,酸性强弱顺序是HCOOH>H2CO3>HCN,故D错误;故选A。

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目