题目内容
氢气是清洁的能源,也是重要的化工原料。
(1)以H2为原料制取氨气进而合成CO(NH2)2的反应如下:
N2(g)+3H2(g)=2NH3(g) △H=―92.40 kJ·mol-1
2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=―159.47 kJ·mol-1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l) △H=+72.49 kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为 。
(2)用丙烷和水为原料在电催化下制氢气,同时得到一种含有三元环的环氧化合物A,该反应的化学方程式为 。该反应也可生成A的同分异构体——另一种环氧化合物B,B的核磁共振氢谱为下图中的 (填“a”或“b”)。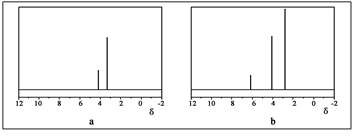
(3)已知叠氮酸(HN3)不稳定,同时也能与活泼金属反应,反应方程式为:
2HN3=3N2↑+H2↑
2HN3+Zn=Zn(N3)2+H2↑
2 mol HN3与一定量Zn完全反应,在标准状况下生成67.2 L气体,其中N2的物质的量为 。
(4)已知H2S高温热分解制H2的反应为:H2S(g) H2(g)+1/2S2(g) 在恒容密闭容器中,控制不同温度进行H2S的分解实验:以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则反应速率v(H2)= (用含c、t的代数式表示)。请说明随温度的升高,曲线b向曲线a逼近的原因: 。
H2(g)+1/2S2(g) 在恒容密闭容器中,控制不同温度进行H2S的分解实验:以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则反应速率v(H2)= (用含c、t的代数式表示)。请说明随温度的升高,曲线b向曲线a逼近的原因: 。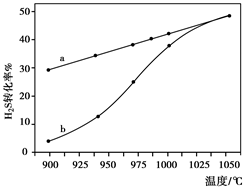
(5)用惰性电极电解煤浆液的方法制H2的反应为:C(s)+2H2O(l)=CO2(g)+2H2(g)现将一定量的1 mol·L-1 H2SO4溶液和适量煤粉充分混合,制成含碳量为0.02 g·mL-1~0.12g·mL-1的煤浆液,置于右图所示装置中进行电解(两电极均为惰性电极)。则A极的电极反应式为 。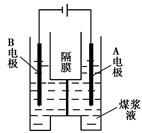
(1)N2(g)+3H2(g)+CO2(g)=CO(NH2)2(s)+H2O(l) △H=-179.38 kJ·mol-1(2分)
(2)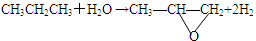 (反应条件可写也可不写)(2分) a(2分)
(反应条件可写也可不写)(2分) a(2分)
(3)2 mol(2分)
(4)0.4c/t mol·L-1·min-1(2分)(单位不写扣1分)
温度升高,反应速率加快,达到平衡所需的时间缩短(合理答案均可)(2分)
(5)C+2H2O-4e-=CO2↑+4H+(2分)
解析试题分析:(1)3个热化学方程式相加得出N2(g)+3H2(g)+CO2(g)=CO(NH2)2(s)+H2O(l) △H=-179.38 kJ·mol-1,(2)三元环的环氧化合物应为2个碳原子1个氧原子的环;另一种环氧化合物应为四元环醚,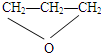 ,图谱为a;(3)根据产生气体的量确定HN3发生两个反应,设两个反应中的量分别为
,图谱为a;(3)根据产生气体的量确定HN3发生两个反应,设两个反应中的量分别为
(3)x、y,有x+y=2 2x+1/2y=67.2÷22.4,解得x=4/3、y=2/3,产生氮气的量为4/3×3/2=2mol;
(4)反应经t min达到平衡,此时H2S的转化率为40%,反应中变化的浓度为0.4cmol·L-1,氢气与H2S变化相同v(H2)=0.4c/t mol·L-1·min-1;温度升高,反应速率加快,达到平衡所需的时间缩短;(5)A电极为阳极,碳失去电子生成二氧化碳,C+2H2O-4e-=CO2↑+4H+。
考点:考查化学反应原理有关问题。

已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题: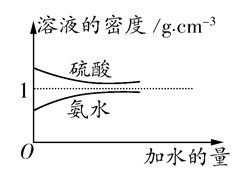
| | 溶质的物质的量 浓度(mol·L-1) | 溶液的密度(g·cm-3) |
| 硫酸 | c1 | ρ1 |
| 氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为 (不写单位,用含c1、ρ1的代数式表示)。
(2)物质的量浓度为c1 mol·L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为 mol·L-1。
(3)物质的量浓度为c2 mol·L-1的氨水与
 c2 mol·L-1的氨水等质量混合,所得溶液的密度 (填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度
c2 mol·L-1的氨水等质量混合,所得溶液的密度 (填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度 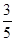 c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
c2 mol·L-1(设混合后溶液的体积变化忽略不计)。 实验室需要0.80 mol·L-1 NaOH溶液475 mL 和0. 40 mol·L-1硫酸500 mL。根据这两种溶液的配制情况回答下列问题: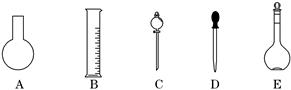
(1)如图所示的仪器中配制溶液肯定不需要的是__________(填编号),配制上述溶液还需用到的玻璃仪器是__________(填仪器名称)。
(2)容量瓶所不具备的功能有__________(填编号)。
| A.配制一定体积准确浓度的标准溶液 |
| B.量取一定体积的液体 |
| C.测量容量瓶规格以下的任意体积的液体 |
| D.贮存溶液 |
(3)根据计算用托盘天平称取NaOH的质量为________g。在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度__________0.80 mol·L-1(填“大于”、“小于”或“等于”,下同)。若还未等溶液冷却就定容了,则所得溶液浓度____________0.80 mol·L-1。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________mL(计算结果保留一位小数)。如果实验室有10 mL、15 mL、20 mL、50 mL的量筒,最好选用________mL的量筒。
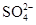 )= ______mol/L。
)= ______mol/L。