题目内容
某同学用12.5 mol/L浓硝酸来配制500 mL1 mol/L的稀硝酸,并进行有关实验。请回答有关问题:
(1)需要量取12.5 mol/L的浓HNO3________mL,配制该稀硝酸时使用的仪器除量筒、玻璃棒、烧杯外,还必须用到的仪器有______、___________等。
(2)取所配制的稀HNO3200 mL,与一定质量的铜粉充分反应,铜粉全部溶解后,生成的唯一还原产物NO气体在标况下的体积为0.56L。则:写出Cu与稀HNO3反应的化学方程式 ,参加反应的铜粉的质量为_________g。
(3)若要将溶液中Cu2+全部转化为Cu(OH)2沉淀,至少需加入0.2mol/L的NaOH溶液的体积为 ml.
(注:要求在答题卡最下面方框内仅列出计算比例式)
(1)40 mL (2分)500mL容量瓶 (2分)胶头滴管 (2分)
(2)3Cu+8HNO3(稀)="=" 3Cu(NO3)2+2NO↑+4H2O ,2.4g(4分);
(3) 875ml.(4分)
解析试题分析:(1)稀释前后溶质的物质的量不变 0.5L×1mol/L=VL×12.5mol/L 所以V=0.04L,既是40ml ,(2)根据方程式中铜和一氧化氮的物质的量之比是3:2,mcu="0.56L/22.4L/mol" ×3/2 ×64g/mol=2.4g (3)根据氮元素守恒,0.2L 1mol/L 既是0.2mol 所以 nNaOH=nNaNO3=0.2mol-nNO=0.175mol 所以VL=n/c=0.175mol/0.2mol/L=0.875L
考点:本题考查了一定物质的量浓度溶液的配制,化学反应方程式的书写及相关物质的量的计算。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案有同学研究从矿石开始到产出钢铁的工艺流程。
(1)将6.62g铁矿石样品投入足量的盐酸中完全溶解后过滤,滤渣中不含铁元素。在滤液中加过量的NaOH溶液,充分反应,过滤、洗涤、灼烧得4.80g Fe2O3。求该铁矿石含铁的质量分数。
(2)现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00吨生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)
(3)取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况)。计算此钢样粉末中铁和碳的物质的量之比。
(4)再取三份不同质量的上述钢样粉末,分别加到100mL相同浓度的H2SO4溶液中,充分反应后,测得的实验数据如下表所示:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
| 生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
计算硫酸溶液的物质的量浓度
(5)若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)
 H2(g)+1/2S2(g) 在恒容密闭容器中,控制不同温度进行H2S的分解实验:以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则反应速率v(H2)= (用含c、t的代数式表示)。请说明随温度的升高,曲线b向曲线a逼近的原因: 。
H2(g)+1/2S2(g) 在恒容密闭容器中,控制不同温度进行H2S的分解实验:以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则反应速率v(H2)= (用含c、t的代数式表示)。请说明随温度的升高,曲线b向曲线a逼近的原因: 。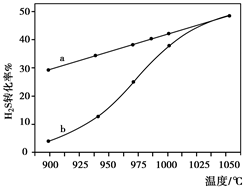


 CO2+2H2O+4Cu。当CH4完全反应后,硬质玻璃管的质量减轻4.8克。将该反应后产生的气体通过过量澄清石灰水中,充分吸收,生成沉淀8.5克。
CO2+2H2O+4Cu。当CH4完全反应后,硬质玻璃管的质量减轻4.8克。将该反应后产生的气体通过过量澄清石灰水中,充分吸收,生成沉淀8.5克。
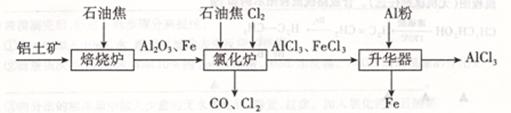
 2Fe(s) +3CO(g);
2Fe(s) +3CO(g);