题目内容
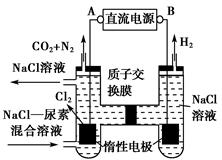
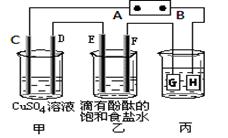
电极a、b分别为Ag电极和Pt电极,电极c、 d都 是 石墨电极。通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体。回答:

(1)直流电源中,M为______________极。
(2)Pt电极上生成的物质是____________,其质量为____________g 。
(3)电子转移的物质的量与电极b、c、d分别生成的物质的物质的量之比为________。
(4)电解过程中,AgNO3溶液的浓度______________(填“增大”、“减小”或“不变”,
下同),AgNO3溶液的pH__________,H2SO4溶液的浓度_________ ,H2SO4溶液的pH________ 。
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为______g。

(1)直流电源中,M为______________极。
(2)Pt电极上生成的物质是____________,其质量为____________g 。
(3)电子转移的物质的量与电极b、c、d分别生成的物质的物质的量之比为________。
(4)电解过程中,AgNO3溶液的浓度______________(填“增大”、“减小”或“不变”,
下同),AgNO3溶液的pH__________,H2SO4溶液的浓度_________ ,H2SO4溶液的pH________ 。
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为______g。
(1)正(1分)
(2)Ag;(1分)2.16(2分)
(3)2:2:0.5:1
(4)不变(1分) 不变(1分)增大(1分)减小(1分)
(5)45.18(2分)
(2)Ag;(1分)2.16(2分)
(3)2:2:0.5:1
(4)不变(1分) 不变(1分)增大(1分)减小(1分)
(5)45.18(2分)
试题分析:(1)左池可认为是镀银装置,所以M为正极,
(2)b极为阴极,发生还原反应,有Ag析出,右池电解产生336ml的气体,其中224ml为氢气,所以转移电子的物质的量为0.02mol,也即有0.02molAg析出,其质量为2.16g;
(3)b极产生0.02molAg,c极为阳极产生氧气0.005mol,d极为阴极产生0.01molH2, 转移电子的物质的量为0.02mol,所以电子转移的物质的量与电极b、c、d分别生成的物质的物质的量之比为2:2:0.5:1;
(4)电解过程中,Ag固体失电子进入溶液,溶液中的Ag+得电子析出,所以AgNO3溶液的浓度不变,溶液的pH不变,右池实质是电解水,所以硫酸溶液浓度增大,pH减小;
(5)由以上分析知电解消耗水的物质的量为0.01mol,质量是0.18g,设原来硫酸溶液的质量为m,则
m ×5%=(m-0.18g) ×5.02%,解得m=45.18g.

练习册系列答案
相关题目

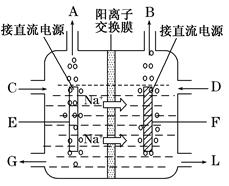
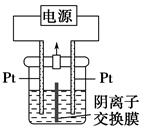
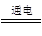 KIO3+3H2↑
KIO3+3H2↑ 

 R2Cu(有机相)+2H+(水相)
R2Cu(有机相)+2H+(水相)