题目内容
7.下列物质中能使品红溶液褪色,加热后溶液又恢复原来颜色的是( )| A. | Cl2 | B. | NO2 | C. | SO2 | D. | H2O2 |
分析 能使品红溶液褪色,加热后溶液又恢复原来颜色,说明该物质的漂白性不稳定,据此分析解答.
解答 解:A.氯气和水反应生成的HClO具有强氧化性,能使品红溶液褪色,且漂白性具有永久性,故A不选;
B.二氧化氮具有强氧化性,能使品红溶液褪色,且漂白性具有永久性,故B不选;
C.二氧化硫和有色物质反应生成无色物质而具有漂白性,但二氧化硫的漂白性具有暂时性特点,受热易恢复原色,故C选;
D.双氧水具有强氧化性,能使品红溶液褪色,且具有永久性,故D不选;
故选C.
点评 本题考查物质的漂白性,明确漂白原理是解本题关键,具有漂白性的物质有臭氧、次氯酸、二氧化硫等,注意二氧化硫的漂白性特点,为易错点.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
17.下列有关Na2CO3和NaHCO3的叙述正确的是( )
| A. | 在相同温度下,Na2CO3比NaHCO3的溶解度小 | |
| B. | 可用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 | |
| C. | 可用加热的方法除去Na2CO3中混有的NaHCO3杂质 | |
| D. | Na2CO3和NaHCO3固体分别与盐酸反应产生等量的CO2时,后者消耗的H+多 |
18.在溶液中能大量共存的一组离子或分子是( )
| A. | NH4+、H+、NO3-、HCO3- | B. | K+、Al3+、SO42-、NH3•H2O | ||
| C. | Na+、K+、SO32-、Cl2 | D. | Na+、Mg2-、SO42-、H+ |
15.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 饱和氯水中:Cl-、NO3-、Na+、CO32- | |
| B. | c(H+)=1.0×10-13mol•L的溶液中:MnO4-、K+、SO42-、AlO2- | |
| C. | c(AlO2-)=1.0mol•L的溶液中:SO42-、K+、Cl-、HCO3- | |
| D. | pH=7的溶液中:NO2-、I-、Na+、Fe3+ |
2.下列反应的能量变化情况符合如图的是( )
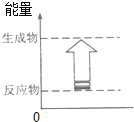

| A. | 石灰石在高温下的分解反应 | B. | 金属钠和水的反应 | ||
| C. | 盐酸与氢氧化钠溶液的反应 | D. | 木炭在氧气中燃烧 |
19.下列叙述正确的是( )
| A. | 纤维素和淀粉互称同分异构体 | B. | 甲烷和异丁烷互称同系物 | ||
| C. | 金刚石和石墨互称同位素 | D. |  和 和 互称同分异构体 互称同分异构体 |
16.下列实验方法或结论叙述正确的是( )
| A. | 用氢氧化钠溶液除去二氧化碳气体中的二氧化硫 | |
| B. | 可用干燥的淀粉碘化钾试纸检验氯气 | |
| C. | 某溶液焰色反应的火焰呈黄色,说明该溶液中肯定含钠离子不确定是否含钾离子 | |
| D. | 用分液漏斗分离水与乙醇的混合物 |

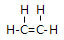 ;由元素④和元素②形成的化合物的电子式为
;由元素④和元素②形成的化合物的电子式为 ;元素⑦的原子结构示意图为
;元素⑦的原子结构示意图为 .
.