题目内容
2.某无色溶液由Mg2+、Al3+、Cl-、NH4+、SO42-中的若干种离子组成.按以下步骤进行实验:(1)取原溶液少量于试管中,向试管中不断加入氢氧化钠溶液至过量,有白色沉淀生成而后又完全消失,说明原溶液中一定含有的离子是Al3+(填相应离子符号,下同).
(2)取实验①后的溶液于另一试管中,加热,用湿润的红色石蕊试纸置于试管口,结果试纸变蓝,说明原溶液中一定含有的离子是NH4+.
(3)取原溶液加入少量盐酸使溶液酸化,再加入氯化钡溶液,产生白色沉淀,说明原溶液中一定含有的离子是SO42-.
(4)取实验③的溶液加入少量,加入硝酸银溶液,产生白色沉淀,能否说明原溶液中一定含有的Cl-离子否(是或否).若要检测Cl-离子是否存在,正确的操作是取原溶液少量于试管中,用硝酸酸化,再滴加硝酸银溶液,若有白色沉淀,证明氯离子存在,否则不含氯离子(若前一格填是,这一格不填).
分析 (1)取原溶液少量于试管中,向试管中不断加入氢氧化钠溶液至过量,有白色沉淀生成而后又完全消失,说明原溶液中一定含有Al3+,一定不含Mg2+;
(2)取实验①后的溶液于另一试管中,加热,用湿润的红色石蕊试纸置于试管口,结果试纸变蓝,应生成氨气,说明含有NH4+;
(3)取原溶液加入少量盐酸使溶液酸化,再加入氯化钡溶液,产生白色沉淀,说明含有SO42-;
(4)取实验③的溶液加入少量,加入硝酸银溶液,产生白色沉淀,说明生成AgCl,但不能说明原溶液含有Cl-,因实验(3)加入氯化钡.
解答 解:(1)取原溶液少量于试管中,向试管中不断加入氢氧化钠溶液至过量,有白色沉淀生成而后又完全消失,说明原溶液中一定含有Al3+,故答案为:Al3+;
(2)取实验①后的溶液于另一试管中,加热,用湿润的红色石蕊试纸置于试管口,结果试纸变蓝,应生成氨气,说明含有NH4+,故答案为:NH4+;
(3)取原溶液加入少量盐酸使溶液酸化,再加入氯化钡溶液,产生白色沉淀,说明含有SO42-,故答案为:SO42-;
(4)取实验③的溶液加入少量,加入硝酸银溶液,产生白色沉淀,说明生成AgCl,但不能说明原溶液含有Cl-,因实验(3)加入氯化钡,若要检测Cl-离子是否存在,正确的操作是取原溶液少量于试管中,用硝酸酸化,再滴加硝酸银溶液,若有白色沉淀,证明氯离子存在,否则不含氯离子,
故答案为:否;取原溶液少量于试管中,用硝酸酸化,再滴加硝酸银溶液,若有白色沉淀,证明氯离子存在,否则不含氯离子.
点评 本题考查物质的检验及鉴别,为高频考点,把握常见离子之间的反应、离子检验等为推断的关键,侧重分析与推断能力的综合考查,题目难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
12.某原电池总反应的离子方程式为:2Fe3++Fe═3Fe2+,能实现该反应的原电池是( )
| A. | 正极为Cu,负极为Fe,电解质溶液为FeCl3溶液 | |
| B. | 正极为C,负极为Fe,电解质溶液为FeSO4溶液 | |
| C. | 正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液 | |
| D. | 正极为Ag,负极为Cu,电解质溶液为CuSO4溶液 |
13.草酸(H2C2O4)是一种二元弱酸,部分性质如下:能溶于水,易溶于乙醇;大约在175℃升华(175℃以上分解生成H2O、CO2和CO);H2C2O4+Ca(OH)2=CaC2O4↓+2H2O.现用H2C2O4进行如下实验:
(一)探究草酸的不稳定性
通过如图1实验装置验证草酸受热分解产物中的CO2和CO,A、B、C中所加入的试剂分别是:
①B中盛装的试剂Ca(OH)2或Ba(OH)2(填化学式);
②A中加入乙醇的目的是除去H2C2O4,避免对CO2的检验造成干扰
(二)探究草酸的酸性
将0.01mol草酸晶体(H2C2O4•2H2O)加入到100mL 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈碱性,其原因是C2O42-+H2O?HC2O4-+OH-(用离子方程式表示).
(三)用酸性KMnO4溶液与H2C2O4溶液反应来探究影响化学反应速率的因素
Ⅰ实验前先用酸性KMnO4标准溶液滴定未知浓度的草酸
反应原理:□MnO${\;}_{4}^{-}$+□H2C2O4+□6H+=□Mn2++□CO2↑+□H2O
①配平上述离子方程式;
②滴定时KMnO4溶液应盛装于酸式(填“酸式”或“碱式”)滴定管中.
Ⅱ探究影响化学反应速率的因素
(1)探究温度对化学反应速率影响的实验编号是②和③(填编号,下同),
探究反应物浓度对化学反应速率影响的实验编号是①和②
(2)测得某次实验(恒温)时溶液中Mn2+物质的量与时间关系如图2.请解释n(Mn2+)在反应起始时变化不大、一段时间后快速增大的原因:Mn2+对该反应有催化作用
(一)探究草酸的不稳定性
通过如图1实验装置验证草酸受热分解产物中的CO2和CO,A、B、C中所加入的试剂分别是:
①B中盛装的试剂Ca(OH)2或Ba(OH)2(填化学式);
②A中加入乙醇的目的是除去H2C2O4,避免对CO2的检验造成干扰
(二)探究草酸的酸性
将0.01mol草酸晶体(H2C2O4•2H2O)加入到100mL 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈碱性,其原因是C2O42-+H2O?HC2O4-+OH-(用离子方程式表示).
(三)用酸性KMnO4溶液与H2C2O4溶液反应来探究影响化学反应速率的因素
Ⅰ实验前先用酸性KMnO4标准溶液滴定未知浓度的草酸
反应原理:□MnO${\;}_{4}^{-}$+□H2C2O4+□6H+=□Mn2++□CO2↑+□H2O
①配平上述离子方程式;
②滴定时KMnO4溶液应盛装于酸式(填“酸式”或“碱式”)滴定管中.
Ⅱ探究影响化学反应速率的因素
| 实验编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度 | ||
| 浓度(mol/L) | 体积(mL) | 浓度(mol/L) | 体积 (mL) | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
探究反应物浓度对化学反应速率影响的实验编号是①和②
(2)测得某次实验(恒温)时溶液中Mn2+物质的量与时间关系如图2.请解释n(Mn2+)在反应起始时变化不大、一段时间后快速增大的原因:Mn2+对该反应有催化作用

10.下列实验的设计可行的是( )
| A. | 用澄清石灰水可区别Na2CO3和NaHCO3粉末 | |
| B. |  用如图装置进行浓硝酸与铜的反应制取并收集NO2 用如图装置进行浓硝酸与铜的反应制取并收集NO2 | |
| C. | 检验未知溶液是否含SO42ˉ可先加氯化钡,再加稀盐酸 | |
| D. | 除去粗盐中的Ca2+、Mg2+、SO42-,可依次加入H2O、NaOH、BaCl2、Na2CO3,过滤再加入HCl |
17.下列各组物质中,互为同位素的是( )
| A. | 氕和氘 | B. | 水(H2O)和重水(D2O) | C. | 氧气和臭氧 | D. | 丁烷和异丁烷 |
14.所有原子都满足最外层8电子稳定结构的化合物分子是( )
| A. | N2 | B. | PCl3 | C. | PCl5 | D. | BeCl2 |
11.一种元素最高价态的氧化物的水化物的化学式为H3XO4,则X的氢化物的化学式是( )
| A. | HX | B. | H2X | C. | XH3 | D. | XH4 |
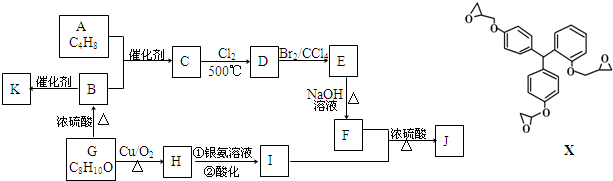
 .
.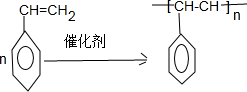 ;F+I→J
;F+I→J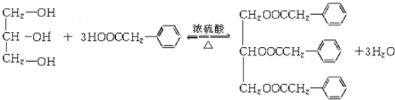 .
. (其中三种).
(其中三种).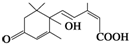 官能团的名称:碳碳双键、羰基、羟基、羧基.
官能团的名称:碳碳双键、羰基、羟基、羧基. 2,3-二甲基戊烷
2,3-二甲基戊烷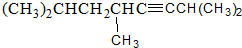 2,5,7-三甲基-3-辛炔
2,5,7-三甲基-3-辛炔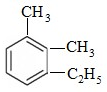
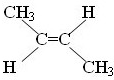 .
.