题目内容
19.燃烧质量相同的下列各有机物时,消耗氧气的量最多的是( )| A. | 乙醇 | B. | 丙醇 | C. | 乙二醇 | D. | 丙三醇 |
分析 令各有机物的质量均为1g,求出其物质的量,再根据燃烧方程式计算.
解答 解:令各有机物的质量均为1g,
A、C2H6O的物质的量为$\frac{1}{46}$mol,则反应消耗的氧气为$\frac{1}{46}$×3=$\frac{3}{46}$mol;
B、C3H8O的物质的量为$\frac{1}{60}$mol,则反应消耗的氧气为$\frac{1}{60}$×4.5=$\frac{4.5}{60}$mol;
C、C2H6O2的物质的量为mol,则反应消耗的氧气为$\frac{1}{62}$×2.5=$\frac{2.5}{62}$mol;
D、C3H8O3的物质的量为$\frac{1}{92}$mol,则反应消耗的氧气为$\frac{1}{92}$×3.5=$\frac{3.5}{92}$;
则消耗氧气的量最多的是C3H6O.
故选:B.
点评 本题考查了烃的含氧衍生物完全燃烧耗氧量问题,难度不大,注意有机物燃烧规律的总结.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
9.将含有0.4mol CuSO4和0.2mol NaCl水溶液1L,用惰性电极电解一段时间后,在一个电极上得到0.3mol Cu,另一电极上析出气体在标况下的体积为( )
| A. | 4.48L | B. | 5.6L | C. | 6.72L | D. | 13.44L |
7.下列是A、B、C、D、E五种元素的某些性质:
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是D.
A.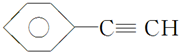 B.CH4
B.CH4
C.CH2═CHCH3 D.CH3CH2C≡CH E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键F-H…F、F-H…O、O-H…F、O-H…O.
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是SO2(化学式),理由是因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大.
(4)B、D形成的氢化物沸点:H2O更高,热稳定性H2O更强.(写化学式)
| A | B | C | D | E | |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
A.
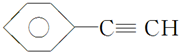 B.CH4
B.CH4C.CH2═CHCH3 D.CH3CH2C≡CH E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键F-H…F、F-H…O、O-H…F、O-H…O.
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是SO2(化学式),理由是因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大.
(4)B、D形成的氢化物沸点:H2O更高,热稳定性H2O更强.(写化学式)
14.分别向含有下列离子的溶液中通入足量NO2气体,数目不会减少的是( )
| A. | SO${\;}_{3}^{2-}$ | B. | CH3COO- | C. | Fe2+ | D. | Al3+ |
8.有关下列图象的分析错误的是( )
| A. | 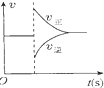 图可表示对平衡N2+3H2?2NH3加压、同时移除部分NH3时的速率变化 | |
| B. | 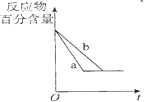 图中a、b曲线只可表示反应H2(g)十I2(g)?2HI(g)在有催化剂和无催化剂存在下建立平衡的过程 | |
| C. | 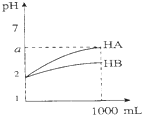 图表示室温下将各1 ml pH=2的HA、HB两种酸溶液加水稀释的情况.若2<a<5,则两酸都为弱酸 | |
| D. | 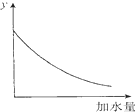 图中的y可表示将O.1 mol/l稀醋酸加水稀释时溶液导电能力的变化情况 |
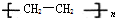 (塑料)、
(塑料)、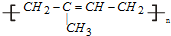 (橡胶).
(橡胶).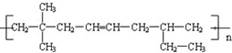 的单体为CH2=C(CH3)2、CH2=CH-CH=CH2、CH2=CHCH2CH3.
的单体为CH2=C(CH3)2、CH2=CH-CH=CH2、CH2=CHCH2CH3. .
.