题目内容
4.按要求填空.(1)已知16g固体硫完全燃烧时放出148.4kJ的热量,该反应的热化学方程式是S(s)+O2(g)=SO2(g);△H=-296.8kJ/mol.
(2)已知拆开1mol H-H键、1mol I-I、分别需要吸收的能量为436kJ、151k J、而形成1mol H-I键会释放299k J能量.则由氢气和碘反应生成1mol HI需要放出(填“放出”或“吸收”)5.5k J的热量.
(3)S(g)+O2(g)=SO2(g)△H1<0;S(s)+O2(g)=SO2(g)△H2<0,比较△H1<△H2大小.
分析 (1)根据热化学方程式的书写方法可知,化学计量数与反应热成正比,并注意标明物质的聚集状态来解答;
(2)化学反应中,化学键断裂吸收能量,形成新化学键放出能量,根据方程式计算分别吸收和放出的能量,以此计算反应热并判断吸热还是放热;
(3)固体硫燃烧时要先变为气态硫,过程吸热.
解答 解:(1)16g固体硫完全燃烧时放出148.4kJ的热量,即1molS完全燃烧时放出放出296.8kj热量,则热化学方程式为:S(s)+O2(g)=SO2(g);△H=-296.8 kJ/mol,
故答案为:S(s)+O2(g)=SO2(g);△H=-296.8 kJ/mol;
(2)在反应H2+I2?2HI中,断裂1molH-H键,1molI-I键共吸收的能量为:1×436kJ+151kJ=587kJ,生成2molHI,共形成2molH-I键,放出的能量为:2×299kJ=598kJ,吸收的能量少,放出的能量多,所以该反应为放热反应,放出的热量为:598kJ-587kJ=11kJ,所以生成1mol HI放出的热量为$\frac{11KJ}{2}$=5.5KJ,
故答案为:放出;5.5;
(3)固体硫燃烧时要先变为气态硫,过程吸热,气体与气体反应生成气体比固体和气体反应生成气体产生热量多,但反应热为负值,所以△H1<△H2;
故答案为:<.
点评 本题考查热化学方程式的书写、反应中热量大小的计算与比较,难度中等,注意盖斯定律的利用,物质的聚集状态不同,反应放出或吸收的热量是不同.

练习册系列答案
相关题目
14.下列有关键线式的说法中错误的是( )
| A. | 将碳、氢元素符号省略,只表示分子中键的连接情况 | |
| B. | 每个拐点、交点、端点均表示有一个碳原子 | |
| C. | 每一条线段代表一个共价键,每个碳原子有四条线段,用四减去线段数即是氢原子数 | |
| D. | C=C、C≡C键等官能团中的“=”和“≡”也可以省略 |
12.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 18gH20中含NA个质子 | |
| B. | 1L 1mol•L一1的CuSO4溶液中含NA个Cu2+ | |
| C. | 常温常压下,2.24L Cl2中含0.2NA个氯原子 | |
| D. | 0.5mol Al与足量NaOH溶液充分反应,转移的电子数目为1.5NA |
19.燃烧质量相同的下列各有机物时,消耗氧气的量最多的是( )
| A. | 乙醇 | B. | 丙醇 | C. | 乙二醇 | D. | 丙三醇 |
9. 氮是地球上含量丰富的一种元素,氮及其化合物在工 农业生产、生活中有着重要作用,
氮是地球上含量丰富的一种元素,氮及其化合物在工 农业生产、生活中有着重要作用,
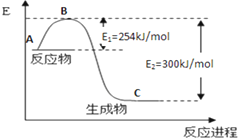
(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:N2(g)+3H2(g)=2NH3(g)△H=-92.2KJ/mol.
(2)若已知下列数据:
试根据表中及图中数据计算N-H的键能390kJ•mol-1.
(3)合成氨反应通常用铁触媒作催化剂.使用铁触媒后△H不变 (填“增大”、“减小”、“不变”)
(4)用NH3催化还原NOX 氮氧化物的污染.例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=akJ•mol-1
N2(g)+O2(g)=2NO(g)△H2=bkJ/mol
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=$\frac{a-3b}{4}$kJ/mol(用含a、b的式子表示)
 氮是地球上含量丰富的一种元素,氮及其化合物在工 农业生产、生活中有着重要作用,
氮是地球上含量丰富的一种元素,氮及其化合物在工 农业生产、生活中有着重要作用,(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:N2(g)+3H2(g)=2NH3(g)△H=-92.2KJ/mol.
(2)若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ•mol-1 | 435 | 943 |
(3)合成氨反应通常用铁触媒作催化剂.使用铁触媒后△H不变 (填“增大”、“减小”、“不变”)
(4)用NH3催化还原NOX 氮氧化物的污染.例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=akJ•mol-1
N2(g)+O2(g)=2NO(g)△H2=bkJ/mol
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=$\frac{a-3b}{4}$kJ/mol(用含a、b的式子表示)
16.下列表示元素的基态原子的电子排布式,其中表示的元素属于第三周期的元素的是( )
| A. | 1s22s1 | B. | 1s22s22p5 | ||
| C. | 1s22s22p63s2 | D. | 1s22s22p63s23p64s1 |
13.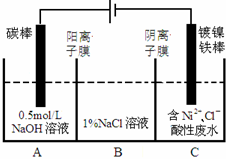 工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是已知:
工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是已知:
①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)( )
 工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是已知:
工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)( )
| A. | 碳棒上发生的电极反应:4OH--4e-═O2↑+2H2O | |
| B. | 为了提高Ni的产率,电解过程中需要控制废水pH | |
| C. | 电解过程中,B中NaCl溶液的物质的量浓度将不断减小 | |
| D. | 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变 |
 实验室可用如图所示装置进行多个实验探究,请回答下列问题.
实验室可用如图所示装置进行多个实验探究,请回答下列问题.