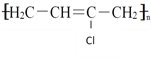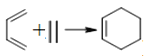题目内容
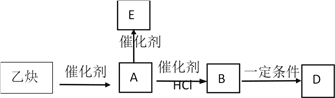
【题目】金刚烷(Ⅰ)、乙二醛、丙二醛均是化工原料,某小组设计的合成路线如下:
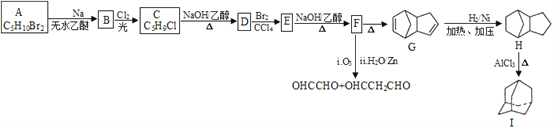
已知:
①2R-Br+2Na![]() R-R+2NaBr
R-R+2NaBr
②B的核磁共振氢谱只有1个吸收峰
③![]()
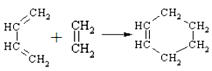
④![]()
回答下列问题:
(1)A的化学名称为_____________; D的结构简式为__________________;I的分子式为__________________。
(2)B→C的化学方程式_________________;E→F的化学方程式为_______________。该反应类型为________________。
(3)G的芳香族同分异构体中,苯环上的取代基数目小于3且能使溴的四氯化碳溶液褪色的共有_______种(不含立体异构);其中核磁共振氢谱有5组峰,且峰面积比为6:2:2:1:1的是_________________(写结构简式)。
(4)写出用环戊二烯和乙烯为原料制备化合物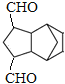 的合成路线____________(其他试剂任选)。
的合成路线____________(其他试剂任选)。
【答案】 1,5-二溴戊烷 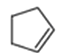 C10H16
C10H16 ![]()
![]() 消去反应 20
消去反应 20 ![]()
【解析】分析:A的分子式为C5H10Br2,A为饱和二溴代烃,A与Na发生题给已知①的反应生成B,B与Cl2光照发生取代反应生成C,C的分子式为C5H9Cl,C中碳原子数与A中碳原子数相等,则B的分子式为C5H10,B属于环烷烃,B的核磁共振氢谱只有1个吸收峰,B的结构简式为![]() ,C的结构简式为
,C的结构简式为![]() ,A的结构简式为BrCH2CH2CH2CH2CH2Br;C与NaOH/乙醇共热发生消去反应生成D,D的结构简式为
,A的结构简式为BrCH2CH2CH2CH2CH2Br;C与NaOH/乙醇共热发生消去反应生成D,D的结构简式为![]() ;D与Br2/CCl4发生加成反应生成E,E的结构简式为
;D与Br2/CCl4发生加成反应生成E,E的结构简式为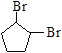 ,E与NaOH/乙醇共热发生消去反应生成F,F的结构简式为
,E与NaOH/乙醇共热发生消去反应生成F,F的结构简式为![]() 。F发生题给已知③的反应生成G,发生题给已知④的反应生成OHCCHO和OHCCH2CHO。
。F发生题给已知③的反应生成G,发生题给已知④的反应生成OHCCHO和OHCCH2CHO。
详解:A的分子式为C5H10Br2,A为饱和二溴代烃,A与Na发生题给已知①的反应生成B,B与Cl2光照发生取代反应生成C,C的分子式为C5H9Cl,C中碳原子数与A中碳原子数相等,则B的分子式为C5H10,B属于环烷烃,B的核磁共振氢谱只有1个吸收峰,B的结构简式为![]() ,C的结构简式为
,C的结构简式为![]() ,A的结构简式为BrCH2CH2CH2CH2CH2Br;C与NaOH/乙醇共热发生消去反应生成D,D的结构简式为
,A的结构简式为BrCH2CH2CH2CH2CH2Br;C与NaOH/乙醇共热发生消去反应生成D,D的结构简式为![]() ;D与Br2/CCl4发生加成反应生成E,E的结构简式为
;D与Br2/CCl4发生加成反应生成E,E的结构简式为 ,E与NaOH/乙醇共热发生消去反应生成F,F的结构简式为
,E与NaOH/乙醇共热发生消去反应生成F,F的结构简式为![]() 。
。
(1)A的结构简式为BrCH2CH2CH2CH2CH2Br,根据系统命名原则,A的化学名称为1,5—二溴戊烷。D的结构简式为![]() 。I的结构简式为
。I的结构简式为![]() ,I的分子式为C10H16。
,I的分子式为C10H16。
(2)B→C的化学方程式为![]() +Cl2
+Cl2![]()
![]() +HCl。E→F的化学方程式为
+HCl。E→F的化学方程式为 +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O,该反应的反应类型为消去反应。
+2NaBr+2H2O,该反应的反应类型为消去反应。
(3)G的结构简式为![]() ,G的分子式为C10H12,G的不饱和度为5;G的芳香族同分异构体中,苯环上取代基数目小于3且能使溴的四氯化碳褪色的有以下情况:①苯环上只有1个取代基,取代基的结构简式有:-CH=CHCH2CH3、-CH2CH=CHCH3、-CH2CH2CH=CH2、
,G的分子式为C10H12,G的不饱和度为5;G的芳香族同分异构体中,苯环上取代基数目小于3且能使溴的四氯化碳褪色的有以下情况:①苯环上只有1个取代基,取代基的结构简式有:-CH=CHCH2CH3、-CH2CH=CHCH3、-CH2CH2CH=CH2、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,共8种;②苯环上有2个取代基,2个取代基的结构简式为:-CH=CHCH3和-CH3、-CH2CH=CH2和-CH3、
,共8种;②苯环上有2个取代基,2个取代基的结构简式为:-CH=CHCH3和-CH3、-CH2CH=CH2和-CH3、![]() 和-CH3、-CH=CH2和-CH2CH3,苯环上的2个取代基有邻、间、对三种位置,共4
和-CH3、-CH=CH2和-CH2CH3,苯环上的2个取代基有邻、间、对三种位置,共4![]() 3=12种;符合题意的同分异构体共8+12=20种。其中核磁共振氢谱有5组峰,且峰面积比为6:2:2:1:1的是
3=12种;符合题意的同分异构体共8+12=20种。其中核磁共振氢谱有5组峰,且峰面积比为6:2:2:1:1的是![]() 。
。
(4)环戊二烯的结构简式为![]() ,对比
,对比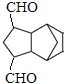 和
和![]() 、CH2=CH2的结构简式,利用题给已知③构建碳干骨架,利用题给已知④得到-CHO。
、CH2=CH2的结构简式,利用题给已知③构建碳干骨架,利用题给已知④得到-CHO。![]() 与CH2=CH2发生题给已知③反应生成
与CH2=CH2发生题给已知③反应生成![]() ,
,![]() 与
与![]() 发生题给已知③反应生成
发生题给已知③反应生成![]() ,
,![]() 发生题给已知④的反应生成
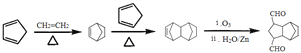
发生题给已知④的反应生成 ,合成路线为:
,合成路线为:![]()
![]()
![]()
![]()
![]()
![]()
 。
。

【题目】硫酸铅可用于铅蓄电池、纤维增重剂、涂料分析试剂。工业上通常用方铅矿(主要成分为PbS)生产硫酸铅。工艺流程如下:

已知:
①25℃,Ksp(PbS)=1.0×10-28,Ksp(PbCl2)=1.6×10-5
②PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq) △H>0
PbCl42-(aq) △H>0
③Fe3+以氢氧化物形式开始沉淀时的pH值为1.9
(1)由于Ksp(PbS)﹤Ksp(PbCl2),PbS+2HCl![]() PbCl2+H2S的反应程度很小,加入FeCl3能增大反应程度,原因是____________________;步骤①反应过程中可观察到有淡黄色固体生成,总反应的离子方程式为_____________________;该步骤需控制溶液的pH<1.9,主要目的是_______________________。
PbCl2+H2S的反应程度很小,加入FeCl3能增大反应程度,原因是____________________;步骤①反应过程中可观察到有淡黄色固体生成,总反应的离子方程式为_____________________;该步骤需控制溶液的pH<1.9,主要目的是_______________________。
(2)步骤②中饱和食盐水的作用是_________________________。
(3)步骤③中滤液A经过蒸发浓缩、用冰水浴冷却结晶后,还需进行的操作是__________(填操作名称)。
(4)步骤④中,若加入稀硫酸充分反应后所得悬浊液中c(Cl-)=1.0mol·L-1,则c(SO42-)=________[Ksp(PbSO4)=1.6×10-8]。步骤⑤中滤液B用适量试剂X处理后可循环利用,试剂X应选用下列中的_____(填标号)。
a.HNO3 b.Cl2 c.H2O2 d.铁粉
(5)炼铅和用铅都会使水体因重金属铅的含量增大而造成严重污染。水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-。各形态的铅浓度分数x与溶液pH变化的关系如图所示:

①探究Pb2+的性质:向含Pb2+的溶液中逐滴滴加NaOH溶液后先变浑浊,继续滴加NaOH溶液又变澄清,pH为13~14时,溶液中发生的主要反应的离子方程式为__________________。
②除去溶液中的Pb2+:科研小组用一种新型试剂(DH)“捕捉”金属离子,从而去除水中的痕量铅和其他杂质离子,实验结果记录如下:
离子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ |
处理前浓度/(mg·L-l) | 0.100 | 29.8 | 0.12 | 0.087 |
处理后浓度/(mg· L-1) | 0.004 | 22.6 | 0.04 | 0.053 |
若新型试剂(DH)在脱铅过程中主要发生的反应为:2DH(s)+Pb2+(aq)![]() D2Pb(s)+2H+(aq),则脱铅时最合适的pH约为_____________。该实验中铅的脱除率为_________________。
D2Pb(s)+2H+(aq),则脱铅时最合适的pH约为_____________。该实验中铅的脱除率为_________________。