题目内容
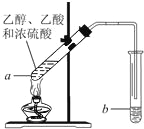
【题目】I. E的产量是衡量一个国家石油化工水平发展的标志,F为高分子化合物,能进行如图所示的反应。

(1)请写出E的电子式_______________。
(2)下列反应的化学方程式:(要求有机物必须写结构简式)
反应②:________________________ 反应类型________。
反应③:________________________ 反应类型________。
反应④:____________________反应类型________。
反应⑤:____________________反应类型________。
(3)比较反应①剧烈程度_____________(填>、= 或<)钠和水反应的剧烈程度。
Ⅱ.2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭。“亮菌甲素”的结构简式为:

它配以辅料丙二醇溶成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性。请回答下列问题:
(1)下列有关“亮菌甲素”的叙述正确的是________(填字母)。
A.“亮菌甲素”能与H2发生加成反应 B.不能使酸性KMnO4溶液褪色
C.“亮菌甲素” 的分子式是C12H10O5 D.“亮菌甲素”分子中含氧官能团只有2种
(2)丙二醇的分子式是C3H8O2,已知两个羟基连在同一个碳原子上的物质不存在。写出其所有属于醇类的同分异构体的结构简式_______________________________。
(3)依据核磁共振氢谱分析,二甘醇分子中有3个吸收峰,其峰面积之比为2∶2∶1。又知二甘醇中含碳、氧元素的质量分数相同,且氢元素的质量分数为9.4%,1 mol二甘醇与足量金属钠反应生成1 mol H2。写出二甘醇的结构简式________________________。
【答案】 ![]()
![]() 加成反应
加成反应 ![]() 酯化反应或取代反应
酯化反应或取代反应 ![]() 氧化反应
氧化反应 ![]() 加聚反应 < AC
加聚反应 < AC ![]() HOCH2CH2OCH2CH2OH
HOCH2CH2OCH2CH2OH
【解析】 I.乙烯的产量是衡量一个国家石油化工水平发展的标志,E为乙烯,A为乙醇,B为乙醇钠, C乙酸乙酯, D为乙醛, F聚乙烯;
(1)正确答案:![]()
(2)②乙烯水化制乙醇,加成反应;正确答案:
![]() ;加成反应;
;加成反应;
③ 乙酸和乙醇在浓硫酸作用下发生酯化反应,生成酯;正确答案:![]() ;酯化反应或取代反应;
;酯化反应或取代反应;
④乙醇在铜作催化剂的条件下,氧化为乙醛;正确答案:
![]() 氧化反应;
氧化反应;
⑤乙烯在一定条件下,发生加聚反应生成聚乙烯;正确答案:
![]() ;加聚反应;
;加聚反应;
(3)醇中羟基中的氢原子比水中羟基中氢活泼性差,因此反应缓慢;正确答案: <
Ⅱ.(1)苯环与氢气发生加成反应,A正确;苯酚、酚羟基、醇羟基都能被酸性KMnO4溶液氧化,B错误;分子式是C12H10O5,C正确;含氧官能团有羟基、羰基、酯基三种,D错误;正确选项:AC;
(2)根据题给信息:满足条件的有2种;正确答案:![]()
(3)二甘醇中氢元素的质量分数为9.4%,含碳、氧元素的质量分数相同各为,碳、氢、氧原子的个数比:(45.3%÷12):(9.4%÷1):(45.3%÷16)=4:10:3,即分子式为C4H10O3,,1 mol二甘醇与足量金属钠反应生成1 mol H2,说明分子结构中含有2个羟基;二甘醇分子中有3个吸收峰,其峰面积之比为2∶2∶1二甘醇的结构简式HOCH2CH2OCH2CH2OH;正确答案:HOCH2CH2OCH2CH2OH;

【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、n、p是由这些元素组成的二元化合物,W2、X2、Z2分别是元素W、X、Z的单质。己知:Ⅰ.一定条件下某密闭容器中可发生反应:aX2+bW2![]() cm,反应过程中物质的浓度变化如下:
cm,反应过程中物质的浓度变化如下:
X2 | W2 | m | |
起始浓度/mol·L-1 | 0.4 | 0.4 | 0 |
平衡浓度/ mol·L-1 | 0.3 | 0.1 | 0.2 |
Ⅱ.它们可发生如下反应:2m(g)+3Z2(g)=6n(g)+X2(g);4n(g)+Y2(g)![]() 2p(l)+2Z2(g)。下列说法正确的是
2p(l)+2Z2(g)。下列说法正确的是
A. 原子半径:W<X<Y B. m、n、p三种物质均为共价化合物
C. X的氧化物一定是无色气体 D. a:b:c=3:1:2