题目内容
【题目】1,6-己二酸(G)是合成尼龙的主要原料之一,可用烃A氧化制备。制备G的合成路线如下:
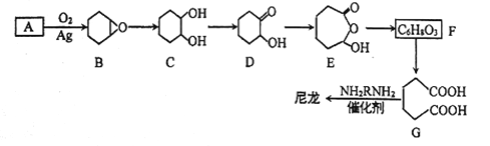
回答下列问题:
(1)化合物A的质谱图如下,则A的化学名称为_______________。
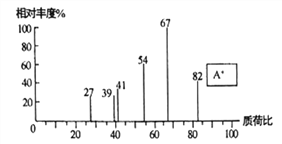
(2)C→D的反应类型为_____________。
(3)F的结构简式为_________________。
(4)写出能同时满足下列条件的X的同分异构体的结构简式______________。
①相对分子质量与F相等
②烃的含氧衍生物,能发生银镜反应
③核磁共振氢谱中有三组峰,面积比为3:2:1
(5)由G合成尼龙的化学方程式为____________________。
(6)由A通过两步反应制备1,3-环己二烯的合成路线为__________________。
【答案】 环已烯 氧化反应 ![]() OHCCH2C(CH3)2CH2CHO、OHCC(CH2CH3)2CHO
OHCCH2C(CH3)2CH2CHO、OHCC(CH2CH3)2CHO ![]()
【解析】试题分析:由A的质谱图及A到B的转化可知,A为环己烯,由F的分子式及E和G的分子结构可知F为![]() ,最后G与某二胺发生缩聚反应得到尼龙。
,最后G与某二胺发生缩聚反应得到尼龙。
(1)由化合物A的质谱图可知,烃A的相对分子质量为82,A可以氧化为B,则A的化学名称为环己烯。
(2)C→D的反应类型为氧化反应。
(3)F的结构简式为![]() 。
。
(4)①相对分子质量与F相等;②烃的含氧衍生物,能发生银镜反应,说明分子中有醛基;③核磁共振氢谱中有三组峰,面积比为3:2:1。能同时满足这些条件的X的同分异构体有OHCCH2C(CH3)2CH2CHO、OHCC(CH2CH3)2CHO。
(5)由G合成尼龙的化学方程式为![]() 。
。
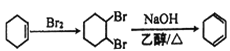
(6)由A(环己烯)通过两步反应制备1,3-环己二烯,首先将环己烯与溴发生加成反应得到1,2-二溴环己烷,然后1,2-二溴环己烷再发生消去反应即可得到产品。具体合成路线如下: 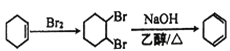 。
。

 培优三好生系列答案
培优三好生系列答案【题目】下列有关物质检验的实验结论正确的是
选项 | 实 验 操 作 及 现 象 | 实 验 结 论 |
A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
B | 向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有 Fe2+ |
C | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
D | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该钾盐是K2CO3 |
A. A B. B C. C D. D
【答案】B
【解析】
白色沉淀可能为AgCl;产生的气体能使澄清石灰水变浑浊,气体为二氧化碳或二氧化硫;先加入硫氰化钾溶液,溶液不显示红色,说明溶液中不存在铁离子,再加入具有氧化性的氯水,溶液变成红色,说明原溶液中一定存在亚铁离子;能使品红褪色的气体不一定为SO2;产生的气体能使澄清石灰水变浑浊,气体为二氧化碳或二氧化硫。
白色沉淀也可能为AgCl,若先加盐酸排除干扰,不生成沉淀,再加氯化钡生成沉淀,则溶液中一定含有SO42-,A错误;向某溶液中加入2滴KSCN溶液,溶液不显红色,说明溶液中不存在铁离子;再向溶液中加入几滴新制的氯水,溶液变为红色,说明加入氯水后溶液中出现了铁离子,证明原溶液中一定含有Fe2+,B正确;能使品红褪色的气体不一定为SO2,也可能为其它强氧化性气体,如氯气、臭氧等,C错误;产生的气体能使澄清石灰水变浑浊,气体可能为二氧化碳或二氧化硫,则溶液中可能含有CO32-、HCO3-,或SO32-、HSO3-,D错误。
【点睛】
本题考查化学实验方案的评价,侧重分析与实验能力的考查,注意实验的评价性分析,把握常见离子的检验、物质的性质、气体的检验等为解答的关键。
【题型】单选题
【结束】
17
【题目】在铜与浓硫酸的反应中,如果转移0.4mol电子,则被还原的硫酸物质的量
A. 0.4mol B. 0.2mol
C. 小于0.4mol D. 小于0.2 mol