题目内容
2.有两个无标签的试剂瓶,分别装有Na2CO3和NaHCO3,有4位同学为鉴别它们采用了以下不同的方法,其中最可行的是( )| A. | 分别配成溶液,再加入澄清石灰水 | |
| B. | 分别配成溶液,再加入CaCl2溶液 | |
| C. | 分别加热,再检验是否有使澄清石灰水变浑浊的气体产生 | |
| D. | 分别配成溶液,再进行焰色反应 |
分析 NaHCO3不稳定,加热易分解,与酸反应较Na2CO3剧烈,二者都能与澄清石灰水反应生成沉淀,因都含有钠元素,焰色反应都呈黄色.
解答 解:A.二者都能与澄清石灰水反应生成沉淀,不能鉴别,故A不选;
B.Na2CO3与CaCl2反应生成白色沉淀,碳酸氢钠不能,能鉴别,且操作简单,故B选;
C.NaHCO3不稳定,加热易分解,生成气体可使澄清石灰水变浑浊,可鉴别,但操作较繁琐,故C不选;
D.都含有钠元素,焰色反应都呈黄色,不能鉴别,故D不选;
故选B.
点评 本题考查碳酸钠与碳酸氢钠的性质探究,侧重于基础知识的考查,题目难度不大,注意把握二者性质的异同,易错点为C,注意反应现象的把握.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
13.下列各组离子中,相互间不能发生复分解反应的是( )
| A. | Mg2+、NH4+、SO42-、Cl- | B. | Cu2+、Na+、HCO3-、OH- | ||
| C. | K+、Ca2+、NO3-、CO32- | D. | Ag+、Fe3+、Cl-、NO3- |
10.下列叙述正确的是( )
| A. | 1摩尔任何物质都含有6.02×1023个分子 | |
| B. | 摩尔是国际单位制中7个基本物理量之一 | |
| C. | 含有6.02×1023个氧原子的H3PO4的物质的量是0.25mol | |
| D. | 氧气的摩尔质量等于它的相对原子质量 |
17.在水溶液中能电离出大量Al3+的电解质是( )
| A. | NaAlO2 | B. | KAl(SO4)2•12H2O | C. | Al(OH)3 | D. | Al2O3 |
7.下列有关氧化还原反应的叙述正确的是( )
| A. | 有单质参加或有单质生成的反应一定是氧化还原反应 | |
| B. | 金属单质参与氧化还原反应时一定作还原剂 | |
| C. | 失去电子难的原子获得电子就一定容易 | |
| D. | 含最高价元素的化合物一定具有强氧化性 |
14.下面是某学生利用数据分析的情况,其中不正确的是( )
| A. | 根据气体的相对分子质量,可以比较相同状况下气体密度的大小 | |
| B. | 根据甲烷和乙烷的熔点,可以比较二者晶体中的分子间作用力的大小 | |
| C. | 比较同周期金属元素原子半径的大小,可以推断元素的金属性强弱 | |
| D. | 根据液体密度的大小,可以判断液体的挥发性的强弱 |
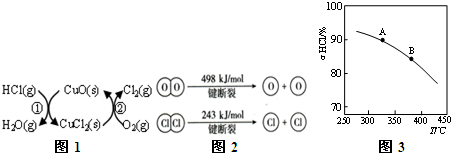
 ,反应A的热化学方程式是4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol.
,反应A的热化学方程式是4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol.