题目内容
4.使溶液中的AlO2-完全转化成Al(OH)3,应选择的最好试剂是( )| A. | 盐酸 | B. | 硫酸 | C. | CO2 | D. | 氨水 |
分析 AlO2-可以和酸反应生成氢氧化铝,Al(OH)3是两性氢氧化物,能溶于强酸、强碱,故制备氢氧化铝时要用弱酸或弱碱.
解答 解:A、由于盐酸是强酸溶液,沉淀AlO2-时生成的氢氧化铝,氢氧化铝能溶解在过量的强酸溶液中,故AlO2-难以完全反应生成氢氧化铝,故A不是最好的试剂 故A错误;
B、硫酸也为强酸,氢氧化铝也能溶于硫酸,故硫酸也不是最好的试剂,故B错误;
C、二氧化碳溶于水生成碳酸,可以与AlO2-反应制备氢氧化铝,故C正确;
D、氨水是弱碱溶液,不与AlO2-反应,故D错误.
故选C.
点评 本题考查了铝盐、氢氧化铝的性质应用,重点考查氢氧化铝的制备,难度不大.

练习册系列答案
相关题目
14.为检验某溴代烃(R-Br)中的溴元素,进行如下操作,正确的顺序是①加热 ②加入AgNO3溶液 ③取少量该溴代烃 ④加入NaOH溶液 ⑤冷却后加入足量稀HNO3酸化( )
| A. | ③④①⑤② | B. | ③①④②⑤ | C. | ③②①⑤④ | D. | ③④①②⑤ |
15.下列反应过程中的能量变化情况符合如图的是( )
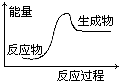

| A. | 酸与碱的中和反应 | B. | 镁和盐酸的反应 | ||
| C. | 氧化钙和水反应 | D. | 水发生分解反应 |
9.实验室欲使1.6g氧化铁完全还原,事先应准备的CO在标准状况下的体积为( )
| A. | 672mL | B. | 336mL | C. | 大于672mL | D. | 小于336mL |
 如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题: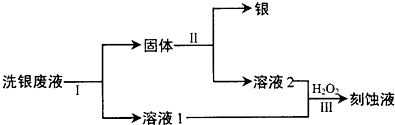
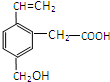 某有机物的结构如图所示,这种有机物不可能具有的性质是
某有机物的结构如图所示,这种有机物不可能具有的性质是