题目内容
14.为检验某溴代烃(R-Br)中的溴元素,进行如下操作,正确的顺序是①加热 ②加入AgNO3溶液 ③取少量该溴代烃 ④加入NaOH溶液 ⑤冷却后加入足量稀HNO3酸化( )| A. | ③④①⑤② | B. | ③①④②⑤ | C. | ③②①⑤④ | D. | ③④①②⑤ |
分析 检验溴乙烷中溴元素,应在碱性条件下加热水解或碱性醇溶液条件下发生消去,最后加入硝酸酸化,加入硝酸银,观察是否有黄色沉淀生成,以此解答.
解答 解:检验溴乙烷中溴元素,应在碱性条件下加热水解或碱性醇溶液条件下发生消去,最后加入硝酸酸化,加入硝酸银,观察是否有黄色沉淀生成,所以操作顺序为③④①⑤②,
故选A.
点评 本题考查溴乙烷的性质以及物质的检验,题目难度中等,易错点为卤代烃水解是碱性溶液中进行,加硝酸银时必须先加酸中和碱才能出现溴化银沉淀,注意实验的操作步骤.

练习册系列答案
相关题目
4. 偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如图,它的化学式是( )
偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如图,它的化学式是( )
 偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如图,它的化学式是( )
偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如图,它的化学式是( )| A. | BaTiO3 | B. | BaTi8O12 | C. | BaTiO4 | D. | BaTi8O4 |
5.已知CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206kJ/mol
CH4(g)+CO2(g)═2CO(g)+2H2 (g)△H=+247kJ/mol
C-H键的键能约为413kJ/mol,O-H键的键能约为463kJ/mol,H-H键的键能约为436kJ/mol,则CO2中C=O键的键能约为( )
CH4(g)+CO2(g)═2CO(g)+2H2 (g)△H=+247kJ/mol
C-H键的键能约为413kJ/mol,O-H键的键能约为463kJ/mol,H-H键的键能约为436kJ/mol,则CO2中C=O键的键能约为( )
| A. | 797.5 kJ/mol | B. | 900.5 kJ/mol | C. | 962.5 kJ/mol | D. | 1595 kJ/mol |
9.下列说法中,正确的是( )
| A. | 天然气的主要成分是乙烯 | |
| B. | 煤焦油分馏可以获得多种芳香烃 | |
| C. | 石油的裂化和裂解都属于物理变化 | |
| D. | 天然气、沼气都属于可再生的清洁能源 |
6.短周期中元素a、b、c在周期表中位置如图所示,下列有关这三种元素的叙述中正确的是( )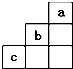

| A. | b的氢化物很稳定 | |
| B. | a是一种活泼的非金属元素 | |
| C. | c的最高价氧化物的水化物是一种弱酸 | |
| D. | b元素在化合物中的最高价为+7价 |
3.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 食盐水和糖水 | B. | 泥沙和水 | C. | 碘和四氯化碳 | D. | 水和四氯化碳 |
4.使溶液中的AlO2-完全转化成Al(OH)3,应选择的最好试剂是( )
| A. | 盐酸 | B. | 硫酸 | C. | CO2 | D. | 氨水 |