题目内容
13.氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图所示:请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是B2O3+3CaF2+3H2SO4 $\frac{\underline{\;\;△\;\;}}{\;}$2BF3↑+3CaSO4+3H2O、B2O3+2NH3$\frac{\underline{\;高温\;}}{\;}$2BN+3H2O;
(2)在BF3分子中,F-B-F的键角是120°,B原子的杂化轨道类型为sp2,BF3和过量NaF作用可生成NaBF4,BF4-的立体结构为正四面体;
(3)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为共价键(或极性共价键),层间作用力为分子间作用力;
(4)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有4个氮原子、4个硼原子,立方氮化硼的密度是$\frac{25×4}{(361.5)^{3}{N}_{A}}$g•cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA).
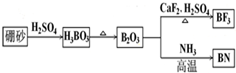
分析 (1)由图及元素守恒可写出这两个反应的方程式;
(2)依据价层电子对互斥理论,计算出的孤对电子对数以及价层电子对数,可判断出分子的空间构型;
(3)B、N均属于非金属元素,二者形成的化学键是极性共价键;根据其结构与石墨相似,层与层之间应该靠分子间作用力结合.
(4)描述晶体结构的基本单元叫做晶胞,金刚石晶胞是立方体,其中8个顶点有8个碳原子,6个面各有6个碳原子,立方体内部还有4个碳原子,如图所示: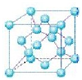 所以金刚石的一个晶胞中含有的碳原子数=8×$\frac{1}{8\frac{(\;\;\;\;)}{(\;\;\;\;)}}$+6×$\frac{1}{2}$+4=8,因此立方氮化硼晶胞中应该含有4个N和4个B原子,一个晶胞中的质量为$\frac{25g}{N{\;}_{A}}$,根据$ρ=\frac{m}{V}$计算密度.
所以金刚石的一个晶胞中含有的碳原子数=8×$\frac{1}{8\frac{(\;\;\;\;)}{(\;\;\;\;)}}$+6×$\frac{1}{2}$+4=8,因此立方氮化硼晶胞中应该含有4个N和4个B原子,一个晶胞中的质量为$\frac{25g}{N{\;}_{A}}$,根据$ρ=\frac{m}{V}$计算密度.
解答 解:(1)由图可知B2O3与CaF2和H2SO4反应即生成BF3,同时还应该产生硫酸钙和水,方程式为B2O3+3CaF2+3H2SO4 $\frac{\underline{\;\;△\;\;}}{\;}$2BF3↑+3CaSO4+3H2O;B2O3与氨气在高温下反应即生成BN,方程式为B2O3+2NH3$\frac{\underline{\;高温\;}}{\;}$2BN+3H2O;
故答案为:B2O3+3CaF2+3H2SO4 $\frac{\underline{\;\;△\;\;}}{\;}$2BF3↑+3CaSO4+3H2O;B2O3+2NH3$\frac{\underline{\;高温\;}}{\;}$2BN+3H2O;
(2)依据价层电子对互斥理论,计算出BF3的孤对电子对数=$\frac{1}{2}$×(a-xb)=$\frac{1}{2}$×(3-3×1)=0,并且价层电子对数为3,所以BF3分子为平面正三角形结构,键角为120°,杂化方式为sp2;BF4-中心原子的孤对电子对数=$\frac{1}{2}$×(a-xb)=$\frac{1}{2}$×(4-4×1)=0,其价层电子对数为4,所以其结构为正四面体,
故答案为:120°;sp2;正四面体;
(3)B、N均属于非金属元素,二者形成的化学键是极性共价键;根据石墨结构可知六方氮化硼晶体中,层与层之间靠分子间作用力结合,
故答案为:共价键(或极性共价键);分子间作用力;
(4)根据金刚石的结构可以判断出金刚石的一个晶胞中含有的碳原子数=8×$\frac{1}{8\frac{(\;\;\;\;)}{(\;\;\;\;)}}$+6×$\frac{1}{2}$+4=8,因此一个立方氮化硼晶胞中含有4个N原子和4个B原子,一个晶胞中的质量为$\frac{25g}{N{\;}_{A}}$,一个立方氮化硼晶胞的体积是(361.5pm)3,因此立方氮化硼的密度是 $\frac{25×4}{(361.5)^{3}{N}_{A}}$g•pm-3,
故答案为:4;4;$\frac{25×4}{(361.5)^{3}{N}_{A}}$•
点评 本题考查较为全面,涉及到化学方程式的书写、电子排布式、分子空间构型、杂化类型的判断以及有关晶体的计算,但解题具有较强的方法性和规律性,学习中注意总结如何书写电子排布式,如何判断分子空间构型以及有关晶体计算等方法.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| 选项 | 化学反应及离子方程式 | 评价 |
| A | AlCl3溶液中加入过量氨水: Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | 错误,铝元素的产物应该是AlO2- |
| B | 过量氯气通入溴化亚铁溶液中: 3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 | 正确 |
| C | 用氨水吸收过量二氧化硫: 2NH3•H2O+SO2═2NH4++SO32-十H2O | 正确 |
| D | 氯化铵溶于水: NH4++2H2O═H3O++NH3•H2O | 错误,氯化铵溶解于水是物理变化,不能写离子方程式 |
| A. | A | B. | B | C. | C | D. | D |
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)②③⑧中形成的简单离子半径由大到小的顺序是Cl->K+>Mg2+.
(3)①和⑨两元素形成的化合物的溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=Br2+2Cl-.
| A. | WZ2分子中所有原子最外层都为8电子结构 | |
| B. | WX2、ZX2的化学键类型相同 | |
| C. | 原子半径大小顺序为X<W<Y<Z | |
| D. | 非金属性Y<Z |
| A. | 氯化铝 | B. | 石蕊 | C. | 亚硫酸钠 | D. | 硝酸银 |
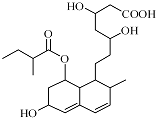
| A. | 能与FeCl3 溶液发生显色反应 | |
| B. | 能使酸性KMnO4 溶液褪色 | |
| C. | 不能发生加成、取代、消去反应 | |
| D. | 1mol 该物质最多可与3mol NaOH 反应 |
( )

| A. | 该样品已完全变质 | |
| B. | 液体丙呈红色或无色 | |
| C. | 该样品中一定含有碳酸钙 | |
| D. | 白色固体甲可能为Ca(OH)2和CaCO3的混合物 |