题目内容
11.设NA为阿伏加德罗常数,下列叙述正确的是( )| A. | 标准状况下,11.2LNO与11.2LO2混合后所含分子数为0.75NA | |
| B. | 0.1molNa2O2晶体中含有0.3NA个离子 | |
| C. | pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA | |
| D. | 标准状况下,22.4L甲醇中含有的氧原子数为1.0NA |
分析 A、11.2LNO与11.2LO2混合后发生的反应为2NO+O2═2NO2,2NO2 N2O4,则反应后的气体的物质的量小于0,75mol;
N2O4,则反应后的气体的物质的量小于0,75mol;
B、Na2O2中含2molNa+和1molO22-;
C、依据体积和氢氧根离子浓度计算物质的量;
D、甲醇在标况下为液态.
解答 解:A、11.2LNO与11.2LO2混合后发生的反应为2NO+O2═2NO2,2NO2 N2O4,则反应后的气体的物质的量小于0,75mol,混合后所含分子数目小于0.75NA,故A错误;
N2O4,则反应后的气体的物质的量小于0,75mol,混合后所含分子数目小于0.75NA,故A错误;
B、Na2O2中含2molNa+和1molO22-,故1molNa2O2中含3mol离子,即3NA个,故B正确;
C、pH=13的1.0LBa(OH)2溶液中,水也能电离出氢氧根离子,所以含有的OH-数目大于0.2NA,故C错误;
D、标况下,甲醇为液态,故不能根据气体摩尔体积来计算,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
2.往Na2S、Na2SO3的混合物中加入稀硫酸,反应中不可能生成的物质是( )
| A. | S | B. | SO2 | C. | H2S | D. | SO3 |
19.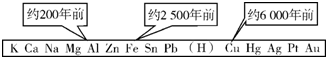 从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平.如图表示了三种金属被人类开发利用的大致年限,金属被利用年限的先后主要取决于( )
从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平.如图表示了三种金属被人类开发利用的大致年限,金属被利用年限的先后主要取决于( )
 从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平.如图表示了三种金属被人类开发利用的大致年限,金属被利用年限的先后主要取决于( )
从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平.如图表示了三种金属被人类开发利用的大致年限,金属被利用年限的先后主要取决于( )| A. | 金属的导电性强弱 | B. | 金属在地壳中的含量多少 | ||
| C. | 金属的化合价高低 | D. | 金属的活动性强弱 |
6.室温下进行的下列实验,不能达到预期目的是序号( )
| 序号 | 实验内容 | 实验目的 |
| A | 测定相同浓度的NaClO溶液,CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| B | 向Mg(OH)2浊液中滴加少量0.1mol/LFeCl3溶液 | 比较Mg(OH)2和Fe(OH)3的溶解度 |
| C | 将两个完全相同且充满NO2的密闭烧瓶,分别浸泡于热水、冰水中 | 探究温度对化学平衡状态的影响 |
| D | 向同体积同浓度H2O2溶液中,分别加入1mol通浓度的CuSO4,FeCl3溶液 | 比较Cu2+、Fe3+对H2O2分解速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
20.常温下,下列说法正确的是( )
| A. | 往CH3COOH溶液中加水,c(OHˉ)和c(H+)均增大 | |
| B. | 物质的量浓度均为0.1mol•Lˉ1的CH3COOH溶液和NaOH溶液等体积混合,c(Na+)<c(CH3COOˉ) | |
| C. | 某浓度的氯化铵溶液中存在c(NH4+)>c(Clˉ)>c(H+)>c(OHˉ) | |
| D. | 在pH=4的氯化铵溶液中c(H+)+c(NH4+)=c(Clˉ)+c(OHˉ) |
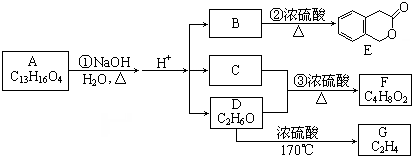
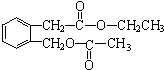 ;B的分子式是C9H10O3.
;B的分子式是C9H10O3. 、
、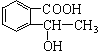 、
、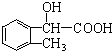 .
. .
. 某学生用如图所示装置证明溴和苯的反应是取代反应而不是加成反应,主要实验步骤如下:
某学生用如图所示装置证明溴和苯的反应是取代反应而不是加成反应,主要实验步骤如下: