题目内容
10. (1)通过火法冶金炼出的铜是粗铜,含杂质多,必须进行电解精炼.请在下面方框中画出电解精炼铜的装置.
(1)通过火法冶金炼出的铜是粗铜,含杂质多,必须进行电解精炼.请在下面方框中画出电解精炼铜的装置.(2)水解反应在生产生活中有很多应用.有些盐水解程度很大,可以用于无机化合物的制备,如可以用TiCl4与H2O反应,生成TiO2•xH2O,制备时加入大量的水,同时加热.请结合化学用语和必要的文字解释“加热”的作用:TiCl4与H2O发生反应:TiCl4+(2+x) H2O=TiO2•xH2O+4HCl,加入大量水并加热,HCl挥发,促使水解正向进行,使水解反应趋于完全,制得TiO2•xH2O.
分析 (1)电解精炼铜时,粗铜作阳极,纯铜作阴极,电解质溶液是含有铜离子的盐溶液;
(2)TiCl4与H2O反应TiCl4+(2+x)H2O=TiO2•xH2O+4HCl,加入大量水并加热,HCl挥发,促使水解正向进行,据此回答.
解答 解:(1)电解精炼铜时,粗铜作阳极,纯铜作阴极,电解质溶液是含有铜离子的盐溶液如硫酸铜溶液,电解装置为: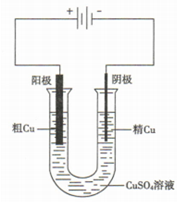 ,故答案为:
,故答案为: ;
;
(2)TiCl4与H2O反应为:TiCl4+(2+x) H2O=TiO2•xH2O+4HCl,加入大量水并加热,HCl挥发,促使水解正向进行,使水解反应趋于完全,制得TiO2•xH2O;
故答案为:TiCl4与H2O发生反应:TiCl4+(2+x) H2O=TiO2•xH2O+4HCl,加入大量水并加热,HCl挥发,促使水解正向进行,使水解反应趋于完全,制得TiO2•xH2O.
点评 本题属于电化学知识的考查题目,涉及电解原理的应用,是一道不错的能力考查题目,要求学生具有扎实的基础与分析、解决问题的能力,难度不大.

练习册系列答案
相关题目
18.常温下,最适宜薄荷生长的土壤pH≈8,土壤中的c(OH-)最接近于( )
| A. | 1×10-5mol/L | B. | 1×10-6mol/L | C. | 1×10-8mol/L | D. | 1×10-9molL |
5.下列用来解释实验事实的相关平衡方程式不正确的是( )
| 实验事实 | 相关平衡方程式 | |
| A | 加入NaHCO3使氯水的漂白能力增强 | Cl2+H2O?HClO+HCl |
| B | 配制FeCl3溶液时加少量盐酸 | Fe3++3OH-?Fe(OH)3 |
| C | 溶有CO2的正常雨水pH=5.6 | H2O+CO2?H2CO3?H++HCO3 |
| D | CaCO3固体溶于盐酸 | CaCO3(s)?Ca2+(aq)+CO32(aq) |
| A. | A | B. | B | C. | C | D. | D |
9.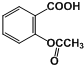 具有解热镇痛作用的阿司匹林的分子结构为如图所示,在一定条件下,阿司匹林可能发生的反应有①取代反应 ②酯化反应 ③银镜反应 ④加成反应 ⑤水解反应 ⑥中和反应( )
具有解热镇痛作用的阿司匹林的分子结构为如图所示,在一定条件下,阿司匹林可能发生的反应有①取代反应 ②酯化反应 ③银镜反应 ④加成反应 ⑤水解反应 ⑥中和反应( )
 具有解热镇痛作用的阿司匹林的分子结构为如图所示,在一定条件下,阿司匹林可能发生的反应有①取代反应 ②酯化反应 ③银镜反应 ④加成反应 ⑤水解反应 ⑥中和反应( )
具有解热镇痛作用的阿司匹林的分子结构为如图所示,在一定条件下,阿司匹林可能发生的反应有①取代反应 ②酯化反应 ③银镜反应 ④加成反应 ⑤水解反应 ⑥中和反应( )| A. | ①②③④⑤ | B. | ①②④⑤⑥ | C. | 全部 | D. | ②④⑤⑥ |
 )广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂内最多
)广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂内最多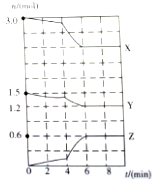
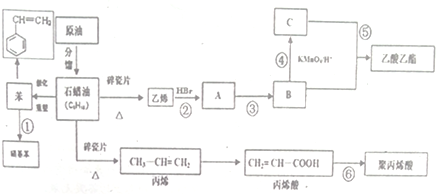
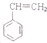 )为原料工业制备苯乙炔(
)为原料工业制备苯乙炔( )的流程如下:
)的流程如下: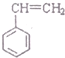 $→_{(1)}^{Br_{2}}$甲$\overrightarrow{(2)}$
$→_{(1)}^{Br_{2}}$甲$\overrightarrow{(2)}$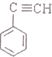
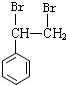
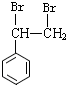 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$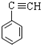 +2NaBr+2H2O
+2NaBr+2H2O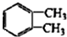 ,其苯环上二氯取代物有三种的芳香烃的名称为对二甲苯或1,4-二甲苯.
,其苯环上二氯取代物有三种的芳香烃的名称为对二甲苯或1,4-二甲苯.