题目内容
17.下列表述中正确的是( )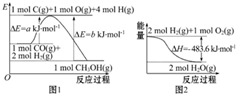
| A. | 根据图1可知合成甲醇的热化学方程式为CO(g)+2H2(g)═CH3OH(g)△H1=(b-a)kJ•mol-1 | |
| B. | 图2表示2 mol H2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ | |
| C. | 1 mol NaOH分别和1 mol 稀硫酸、1 mol浓硫酸反应,前者的△H比后者的△H大 | |
| D. | 汽油燃烧时将全部的化学能转化为热能 |
分析 A.该反应是放热反应,△H为负值;
B.应为反应物的总能量大于生成物的总能量;
C.浓硫酸的稀释放热,中和反应放热,焓变是负值;
D.汽油燃烧时产生热和光,据此回答.
解答 解:A.该反应是放热反应,△H为负值,△H1=(a-b)kJ•mol-1,故A错误;
B.图2表示2 mol H2(g)和1molO2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ,故B错误;
C.浓硫酸的稀释过程是放热的,中和反应的焓变是负值,后者比前者△H小,故C正确;
D.汽油燃烧时产生热和光,将化学能转化为热能和光能,故D错误.
故选C.
点评 本题考查常见的能量转化形式、吸热反应和放热反应,题目难度不大,注意汽油燃烧时产生热和光.

练习册系列答案
相关题目
12.下列有关生活和生产中化学知识的描述正确的是( )
| A. | 高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” | |
| B. | 侯氏制碱法的工艺原理主要应用了物质熔沸点的差异 | |
| C. | 铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝 | |
| D. | 用蘸有浓氨水的玻璃棒检验输送氯气的管道是否漏气 |
9.用下列装置进行相应实验,能达到实验目的是( )
| A. |  配制一定浓度的稀硫酸 | B. | 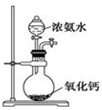 实验室制取氨气 | ||
| C. | 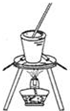 蒸发饱和食盐水 | D. | 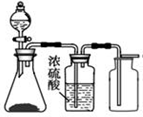 制取、收集氢气 |
6.用Cu和HNO3反应制Cu(NO3)2,应选用的方法是( )
| A. | Cu和浓HNO3反应 | B. | Cu和稀HNO3反应 | ||
| C. | 先把Cu粉氧化,再用稀HNO3溶解CuO | D. | 上述任何方法都一样 |