题目内容
6.用Cu和HNO3反应制Cu(NO3)2,应选用的方法是( )| A. | Cu和浓HNO3反应 | B. | Cu和稀HNO3反应 | ||
| C. | 先把Cu粉氧化,再用稀HNO3溶解CuO | D. | 上述任何方法都一样 |
分析 铜与浓硝酸反应的方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,铜与稀硝酸反应的方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,两个反应中都产生了污染气体;用Cu和HNO3反应制Cu(NO3)2,可先把Cu粉氧化,再用稀HNO3溶解CuO,该方案中没有生成污染气体.
解答 解:A.铜与浓硝酸反应的方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,反应中有二氧化氮产生,既污染环境还造成资源浪费,该方法不可取,故A错误;
B.铜与稀硝酸反应的方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,反应中产生了有毒气体NO,且造成了资源浪费,该方法不可取,故B错误;
C.先把Cu粉氧化生成氧化铜,再用稀HNO3溶解CuO获得硝酸铜和水,该方案中既没有污染物生成,还能够充分利用资源,可用该方案制备硝酸铜,故C正确;
D.选项C的方案合理,而A、B的方案不合理,故D错误;
故选C.
点评 本题考查了硝酸铜的制备方案的判断,题目难度中等,明确铜及其化合物性质为解答关键,注意掌握物质制备方案的设计与评价原则,试题侧重考查学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
1.学习化学关键是掌握一些化学学习方法及学科思想.实验室有一标签残缺的硫酸,怎样确定它是否是浓硫酸,你认为应该选用下述方法中的( )方法.
| A. | 讨论 | B. | 调查 | C. | 观察和实验 | D. | 上网 |
17.下列表述中正确的是( )
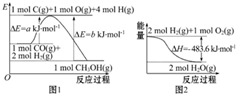

| A. | 根据图1可知合成甲醇的热化学方程式为CO(g)+2H2(g)═CH3OH(g)△H1=(b-a)kJ•mol-1 | |
| B. | 图2表示2 mol H2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ | |
| C. | 1 mol NaOH分别和1 mol 稀硫酸、1 mol浓硫酸反应,前者的△H比后者的△H大 | |
| D. | 汽油燃烧时将全部的化学能转化为热能 |
14.下列装置或操作能达到实验目的是( )


| A. | 分离水和CCl4 | B. | 定容 | ||
| C. | 比较两种盐的热稳定性 | D. | 除去CO的CO2 |
11.除去下列溶液中的杂质(括号内是杂质)所选试剂正确的是( )
| A. | NaOH溶液[Ba(OH)2]:适量Na2SO4溶液 | B. | HNO3溶液[HCl]:过量AgNO3溶液 | ||
| C. | KOH溶液[K2CO3]:适量CaCl2溶液 | D. | Mg[Al]:过量NaOH溶液 |
15.3.84g铜跟一定量的浓硝酸反应,铜消耗完时,共产生标准状况下气体体积2.24L,则消耗的硝酸的物质的量为( )
| A. | 0.20mol | B. | 0.21mol | C. | 0.22mol | D. | 0.23mol |
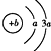 ,Y、Z为同周期金属元素,Y、Z的最高价氧化物对应水化物可以反应生成盐和水.回答下列问题:
,Y、Z为同周期金属元素,Y、Z的最高价氧化物对应水化物可以反应生成盐和水.回答下列问题: