题目内容
【题目】(1)请用化学方程式写出如何检验牙膏中存在甘油的方法___。
(2)Ca3N2是离子化合物,各原子均满足8电子稳定结构。写出Ca3N2的电子式___。
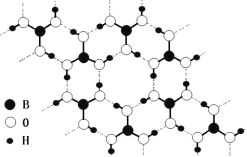
(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图。1mol硼酸(H3BO3)晶体中含有___mol氢键。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:___。
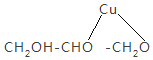
【答案】CH2OH-CHOH-CH2OH+Cu(OH)2![]()
 +2H2O
+2H2O 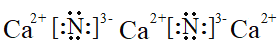 3 H3BO3分子之间形成氢键,使硼酸缔合成层状大分子,在冷水中溶解度小,而热水中H3BO3分子之间形成氢键被破坏,H3BO3分子与水分子之间形成大量的氢键,增大了溶解度
3 H3BO3分子之间形成氢键,使硼酸缔合成层状大分子,在冷水中溶解度小,而热水中H3BO3分子之间形成氢键被破坏,H3BO3分子与水分子之间形成大量的氢键,增大了溶解度
【解析】
(1)甘油与新制氢氧化铜反应生成绛蓝色的溶液,因此可用来检验牙膏中存在甘油,方程式为CH2OH-CHOH-CH2OH+Cu(OH)2![]()
 +2H2O;
+2H2O;
(2)Ca3N2是离子化合物,各原子均满足8电子稳定结构,因此Ca3N2的电子式为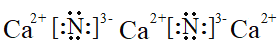 ;
;
(3)1个H3BO3周围形成6个氢键,每个氢键为1个H3BO3贡献率为![]() ,即1个H3BO3单独占有氢键数目为6×
,即1个H3BO3单独占有氢键数目为6×![]() =3,故1mol H3BO3晶体中含有3mol氢键;H3BO3分子之间形成氢键,使硼酸缔合成层状大分子,在冷水中溶解度小,而热水中H3BO3分子之间形成氢键被破坏,H3BO3分子与水分子之间形成大量的氢键,故硼酸在冷水中的溶解度小而加热时溶解度增大。
=3,故1mol H3BO3晶体中含有3mol氢键;H3BO3分子之间形成氢键,使硼酸缔合成层状大分子,在冷水中溶解度小,而热水中H3BO3分子之间形成氢键被破坏,H3BO3分子与水分子之间形成大量的氢键,故硼酸在冷水中的溶解度小而加热时溶解度增大。

练习册系列答案
相关题目