题目内容
1.在现代化学分析测试中,常借助一些仪器来分析化学物质的组成.下列有关说法不正确的是( )| A. | 用红外光谱仪确定物质中是否存在Na+、K+、Cu2+等离子 | |
| B. | 用元素分析仪确定物质中是否含有C、H、O、N、S等 | |
| C. | 用原子吸收光谱确定物质中含有哪些金属元素 | |
| D. | 用pH计来测量溶液的酸碱性 |
分析 A.红外光谱仪可以确定物质中是否存在某些有机原子基团;
B.元素分析仪可测定元素种类;
C.不同元素的原子发生跃迁时会吸收不同的,形成特征谱线;
D.pH计可以测量溶液的酸碱性.
解答 解:A.红外光谱仪是利用物质对不同波长的红外辐射的吸收特性,进行分子结构和化学组成分析的仪器,用红外光谱仪可以确定物质中是否存在某些有机原子基团,不能确定离子,故A错误;
B.元素分析仪作为一种实验室常规仪器,可同时对有机的固体、高挥发性和敏感性物质中C、H、N、S、元素的含量进行定量分析测定,故B正确;
C.不同元素的原子发生跃迁时会吸收不同的,形成特征谱线,所以现代化学分析测试中用原子吸收光谱确定物质中含有哪些金属元素,故C正确;
D.PH计所测量的pH值是用来表示溶液酸碱度的一种方法,它用溶液中的H离子浓度的负对数来表示,故D正确.
故选A.
点评 本题考查物质的检验和鉴别的方法,题目难度不大,对于D来说,我们可能较为陌生,学习中注意开拓视野,加强相关知识的积累.

练习册系列答案
相关题目
11. 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率.
(1)除如图装置所示的实验用品外,还需要的一件实验用品是秒表.
(2)圆底烧瓶中反应现象:溶液变浑浊,并有刺激性气体产生,写出所发生反应的离子方程式为S2O32-+2H+═H2O+S↓+SO2↑.
(3)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是SO2会部分溶于水.
(4)利用该化学反应,试简述测定反应速率的其他方法:测定一段时间内生成硫沉淀的质量(或实时测定溶液中氢离子浓度)(写一种).Ⅱ.探究化学反应速率的影响因素为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表.(已知 I2+2S2O${\;}_{3}^{2-}$═S4O${\;}_{6}^{2-}$+2I-,其中Na2S2O3溶液均足量)
(5)表中Vx=4mL,T1、T2、T3的大小关系是T1<T2<T3.
 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率.
(1)除如图装置所示的实验用品外,还需要的一件实验用品是秒表.
(2)圆底烧瓶中反应现象:溶液变浑浊,并有刺激性气体产生,写出所发生反应的离子方程式为S2O32-+2H+═H2O+S↓+SO2↑.
(3)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是SO2会部分溶于水.
(4)利用该化学反应,试简述测定反应速率的其他方法:测定一段时间内生成硫沉淀的质量(或实时测定溶液中氢离子浓度)(写一种).Ⅱ.探究化学反应速率的影响因素为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表.(已知 I2+2S2O${\;}_{3}^{2-}$═S4O${\;}_{6}^{2-}$+2I-,其中Na2S2O3溶液均足量)
| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | T1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | T2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | T3 |
9.下列说法不正确的是( )
| A. | 氧气和臭氧互为同素异形体 | |
| B. | CH3-CH2OH和 CH3-O-CH3互为同分异构体 | |
| C. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同位素 | |
| D. | ${\;}_{2}^{4}$He的最外层电子数为2,所以${\;}_{2}^{3}$He具有较强的金属性 |
16.为了证明某固体中含有氯离子,选用给出的试剂和操作,其操作顺序正确的是( )
①滴加AgNO3溶液 ②加水溶解 ⑤过滤、取滤液 ④与二氧化锰混合加热 ⑤加稀HNO3 ⑥与浓盐酸反应 ⑦加NaOH溶液加热 ⑧用淀粉碘化钾.
①滴加AgNO3溶液 ②加水溶解 ⑤过滤、取滤液 ④与二氧化锰混合加热 ⑤加稀HNO3 ⑥与浓盐酸反应 ⑦加NaOH溶液加热 ⑧用淀粉碘化钾.
| A. | ④②③①⑤ | B. | ⑥⑧ | C. | ②①⑤ | D. | ⑥⑦①⑤ |
6.将如图所示实验装置的K闭合,下列判断正确的是( )
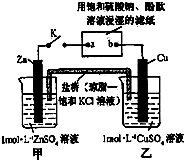

| A. | 片刻后可观察到滤纸a点变红色 | B. | 电子沿Zn→a→b→Cu路径流动 | ||
| C. | 片刻后甲池中c(SO42-)增大 | D. | 盐桥中的Cl-向Cu极移动 |
13.短周期元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族.下列说法正确的是( )
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | X的最高价氧化物对应的水化物的酸性比W的弱 | |
| C. | Y的气态简单氢化物的热稳定性比W的强 | |
| D. | Y分别与Z、W形成的化合物中化学键类型相同 |
10.一个原电池的总反应的离子方程式是Fe+Cu2+═Fe2++Cu,该反应的原电池组成正确的是( )
| A | B | C | D | |
| 正极 | Fe | Fe | Cu | Cu |
| 负极 | Cu | Cu | Fe | Fe |
| 电解质溶液 | CuSO4 | H2SO4 | CuCl2 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
11.N2H4是一种重要的火箭燃料,能在空气中燃烧生成氮气和水,放出大量的热.室温时,已知各共价键的键能如下表,通过计算N2H4的燃烧热是( )
| 键 | N-H | N-N | O=O | N≡N | H-O |
| 键能/kJ•mol-1 | 391 | 193 | 497 | 946 | 463 |
| A. | 1088 kJ•mol-1 | B. | 544 kJ•mol-1 | C. | 790 kJ•mol-1 | D. | 382 kJ•mol-1 |
 为探究溴乙烷与NaOH乙醇溶液发生反应后生成的气体中是否含不饱和烃的装置如图所示.回答:
为探究溴乙烷与NaOH乙醇溶液发生反应后生成的气体中是否含不饱和烃的装置如图所示.回答: