��Ŀ����
����Ŀ������ý����Ҫ�Ĵ�����CO��������ý���õ�����ʧȥ�����ԣ�Fe+5CO=Fe(CO)5����ȥCO�Ļ�ѧ��ӦΪ��[Cu(NH3)2]OOCCH3+CO+NH3��[Cu(NH3)3(CO)]OOCCH3��
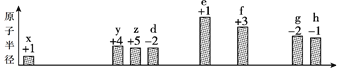
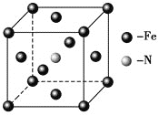
(1)��̬Feԭ�ӵ���Χ�����Ų�ʽ��________��C��N��O�ĵ�һ�������ɴ�С��˳��Ϊ________��
��2��Fe(CO)5�����ʻ�����������Ϊ��ɫ��״Һ�壬��Fe(CO)5�ľ���������_______����CO��Ϊ�ȵ�����ķ��ӵĵ���ʽΪ______________��
��3���������NO3-�Ŀռ乹��_______�������еĴ��������÷���![]() ��ʾ������m���������γɵĴ�����ԭ������n���������γɵĴ��������������籽�����еĴ������ɱ�ʾΪ
��ʾ������m���������γɵĴ�����ԭ������n���������γɵĴ��������������籽�����еĴ������ɱ�ʾΪ![]() ������NO3-�еĴ�����Ӧ��ʾΪ____________��
������NO3-�еĴ�����Ӧ��ʾΪ____________��
��4�������[Cu(NH3)2]OOCCH3��̼ԭ�ӵ��ӻ�������________����λ�����ṩ�¶Ե��ӵ�ԭ����_____��
��5����[Cu(NH3)2]OOCCH3��ȥCO�ķ�Ӧ�У��϶���______�γɣ�
a�����Ӽ� b����λ�� c���Ǽ��Լ� d������
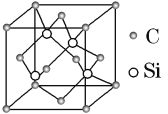
��6�����Ͱ�����640 ���ɷ����û���Ӧ������֮һ�ľ����ṹ��ͼ��ʾ��д���÷�Ӧ�Ļ�ѧ����ʽ__________________ ��
���𰸡� 3d64s2 N��O��C ���Ӿ��� ![]() ƽ��������
ƽ�������� ![]() sp2��sp3 N bd 8Fe+2NH3
sp2��sp3 N bd 8Fe+2NH3![]() 2Fe4N+3H2
2Fe4N+3H2
��������
��1��Feԭ��3d��4s�ܼ�����Ϊ��۵��ӣ���̬Feԭ�ӵļ۵����Ų�ʽΪ3d64s2��ͬһ����Ԫ�أ�Ԫ�ص縺������ԭ������������������ڵ�Ԫ�ص�2p������Ӵ��ڰ����״̬���ȶ���ǿ����һ�����ܴ�������Ԫ�أ���������Ԫ�ص�һ�����ܴ�С˳����N��O��C��
��2���۷е�ϵ͵ľ���Ϊ���Ӿ��壬Fe(CO)5�����ʻ�����������Ϊ��ɫ��״Һ�壬���۷е�ϵͣ�Ϊ���Ӿ��壻ԭ�����ͼ۵������ֱ���ȵĻ�Ϊ�ȵ����壬��CO��Ϊ�ȵ�����ķ����ǵ���������ʽΪ![]() ��
��
��3��NO3-��Nԭ�ӵļ۲���Ӷ�����![]() �������й¶Ե��ӣ�����Ŀռ乹��ƽ����������N��2s�ܼ���һ������ԾǨ��2pz�����2s��2px��2py��������γ�sp2�ӻ������2pz���������һ�Ե��ӣ�ÿ��Oԭ��2pz�������һ�������ӣ��ټ�����������һ����λ����ɣ���NO3-�γ������������ӵ��������������ʾΪ
�������й¶Ե��ӣ�����Ŀռ乹��ƽ����������N��2s�ܼ���һ������ԾǨ��2pz�����2s��2px��2py��������γ�sp2�ӻ������2pz���������һ�Ե��ӣ�ÿ��Oԭ��2pz�������һ�������ӣ��ټ�����������һ����λ����ɣ���NO3-�γ������������ӵ��������������ʾΪ![]() ��
��
��4�����������Cԭ�Ӽ۲���ӶԸ�����4��3�Ҳ����µ��Ӷԣ����ݼ۲���ӶԻ�������ȷ��Cԭ���ӻ���ʽΪsp3��sp2����������Cuԭ���ṩ�չ����Nԭ���ṩ�µ��Ӷԣ��γ���λ����
��5����[Cu(NH3)2]OOCCH3��ȥCO�ķ�Ӧ�У��϶���Cuԭ�Ӻ�N��Cԭ��֮�����λ����Ҳ���������ɣ���Ϊbd��
��6�����þ�̯�����㾧����Feԭ�Ӹ���Ϊ8��1/8+6��1/2��4��Nԭ���ھ����У����Ƶ�1������ѧʽΪFe4N�����ڷ������û���Ӧ������һ�������������������Ը÷�Ӧ�Ļ�ѧ����ʽΪ8Fe+2NH3![]() 2Fe4N+3H2��
2Fe4N+3H2��

����Ŀ��ij��ȤС���Է���м�Ƶ���������狀����������Ʊ���ˮ�ϲ�������(FeC2O4��2H2O)����һ���Ʊ��ߴ��Ȼ�ԭ���ۡ�

��֪��FeC2O4��2H2O������ˮ��150�濪ʼʧ�ᾧˮ��H2C2O4������ˮ���ܽ�����¶����߶�����
��ش�
��1�����в�����������ȷ����__________��
A.����ڣ�H2C2O4�Թ�����Ҫ��Ϊ������Fe2+ˮ��
B.����ۣ�������ˮϴ�ӿ���߳���Ч��
C.����ۣ�ĸҺ�е�������Ҫ��(NH4)2SO4 ��H2C2O4
D.����ۣ�����ڳ�ѹ�¿��ٸ���¶ȿ�ѡ���Ը���100��
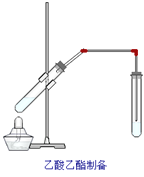
��2����ͼװ�ã�����һϵ�в�����ɲ�����еij��˺�ϴ�ӡ���ѡ����ʵı�ţ�����ȷ�IJ���˳������(ϴ�Ӳ���ֻ�迼��һ��)��
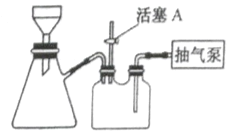
�������á�a��b��d��_________��c���س�����
a.ת�ƹ�Һ���� b.�ػ���A�� c.������A�� d.ȷ�ϳ�ɣ� e.��ϴ�Ӽ�ϴ�ӡ�
��3����ȡһ������FeC2O4��2H2O�������������ܽ⣬����KMnO4�ζ����ⶨ�����������£�
n (Fe2+)/mol | n (C2O42��)/mol | ������FeC2O4��2H2O���������� |
9.80��10��4 | 9.80��10��4 | 0.980 |
�ɱ��������Ʋ�����������Ҫ��������___________
��4��ʵ�ֲ���ܱ����õ�������������_________(��ѡ������a.�ձ���b.������c.������ƿ��d.����¯��e.������f.��ƿ)���ò���Ļ�ѧ����ʽ��______________________��
��5��Ϊʵ�ֲ���ݣ�������̼�ۻ�ԭFe2O3��������________________��