题目内容
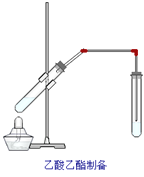
【题目】如图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2 mL乙酸,充分摇匀。在右试管中加入5mL饱和Na2CO3溶液。按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验。
(1)写出左试管中主要反应的方程式:____________________;
(2)加入浓硫酸的作用:_________________________;
(3)饱和Na2CO3的作用是:____________;__________________;__________________。
【答案】CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 催化剂和吸水剂 吸收多余的乙酸 溶解多余的乙醇 降低乙酸乙酯的溶解性
CH3COOCH2CH3+H2O 催化剂和吸水剂 吸收多余的乙酸 溶解多余的乙醇 降低乙酸乙酯的溶解性
【解析】
(1)醋酸和乙醇在浓硫酸催化作用下发生酯化反应,生成乙酸乙酯和水;
(2)浓硫酸做酯化反应的催化剂和吸水剂;
(3)实验室里用饱和碳酸钠溶液吸收乙酸乙酯的原因:一是利用碳酸钠溶液中的水溶解乙醇(乙醇在水里的溶解度大于乙酸乙酯),二是碳酸钠能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,而乙酸乙酯难溶于饱和碳酸钠溶液,这样就可以获得较为纯净的乙酸乙酯液体。
(1)乙酸和乙醇在浓硫酸催化作用下发生酯化反应,生成乙酸乙酯和水,反应的化学方程式为:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(2)浓硫酸有吸水性,促进该反应向正反应方向移动,浓硫酸能加快反应速率,所以浓硫酸作催化剂和吸水剂;
(3)碳酸钠溶液能溶解乙醇,能跟乙酸反应吸收乙酸,降低乙酸乙酯的溶解度,便于分层,故答案为:吸收多余的乙酸、溶解多余的乙醇、降低乙酸乙酯的溶解性。

练习册系列答案
相关题目