题目内容
【题目】物质的结构决定物质的性质。请回答下列涉及物质结构和性质的问题:
(1)氨气极易溶于水的主要原因是_____________________。
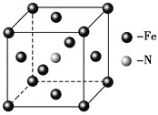
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的外围电子排布式为________________。
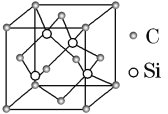
(3)碳化硅的结构与金刚石类似(如图所示),4个硅原子位于体心位置,碳原子位于顶点、面心位置,其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个硅原子周围与其距离最近的碳原子有_______个,碳化硅化学式为________。已知碳化硅晶胞边长为acm,阿伏加德罗常数为NA,则碳化硅的密度为_______g·cm3。
(4)(CH3)3N可用于制备医药、农药,则(CH3)3N_______(填“能”或“不能”)溶于水。化合物(CH3)3N与盐酸反应生成[(CH3)3NH]+,该过程新生成的化学键为_______。
a.离子键 b.配位键 c.氢键 d.非极性共价键
(5)成键原子中的孤电子对对键能有影响,第二周期元素A与氢形成的化合物中A-A键的键能(单位:kJ·mol-1)如下:H3C-CH3 346,H2N-NH2 247,HO-OH 207;
试分析上述化合物中A-A键的键能依次下降的原因__________________________。
【答案】 氨分子间存在氢键 3d84s2 4 SiC 160/NAa3 能 b 孤电子对越多,对成键电子的排斥挤压增强,导致轨道重叠程度减小,成键能力下降,键能下降
【解析】
(1)由于氨分子间存在氢键,因此氨气极易溶于水;
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,碳原子有2个未成对电子,因此该元素是Ni,则其基态原子的外围电子排布式为3d84s2;
(3)4个硅原子位于体心位置,即晶胞中含有4个Si。碳原子位于顶点、面心位置,则晶胞中含有的碳原子个数是8×1/8+6×1/2=4,所以其化学式是SiC。碳化硅晶胞结构中每个硅原子周围与其距离最近的碳原子有4个,以硅原子为中心构成四面体。已知碳化硅晶胞边长为a cm,则其体积是a3 cm3,阿伏加德罗常数为NA,所以碳化硅的密度为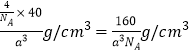 ;
;
(4)极性分子(CH3)3N和水之间能形成氢键,所以(CH3)3N能溶于水。化合物(CH3)3N与盐酸反应生成[(CH3)3NH]+,该过程新生成的化学键为氮与氢离子形成配位键,答案选b;
(5)根据键能数据可知由于孤电子对越多,对成键电子的排斥挤压增强,导致轨道重叠程度减小,成键能力下降,键能下降,因此上述化合物中A-A键的键能依次下降。