题目内容
【题目】室温下,用0.10mol/L CH3 COOH溶液滴定10.00mL浓度均为0.10 mol/L NaOH和NH3·H2O的混合液,混合溶液的相对导电能力随乙酸滴入的变化曲线如下图所示。已知:Ka(CH3COOH)=1. 8×10-5,Kb( NH3·H2O) =1. 8× l0-5。下列叙述错误的是

A.ab段为CH3COOH与NaOH的中和过程
B.b点水的电离程度最大
C.c点3c(Na+)=2c(CH3 COOH)+2c(CH3 COO-)
D.d点c(Na+)>c(NH![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
【答案】B
【解析】
由Ka(CH3COOH)=1. 8×10-5、Kb( NH3·H2O) =1. 8× l0-5可知,在室温下,两种弱电解质的电离常数相同。
A. 由图中信息可知,ab段溶液的导电能力逐渐减弱至最低,说明在此过程中,溶液中的离子总浓度逐渐减小,只是CH3COOH与NaOH的中和过程,NaOH是强碱,其完全电离,故其先参与中和反应,NH3·H2O是弱碱,其没有参加反应,因为只要NH3·H2O参加反应就会生成可溶性的强电解质醋酸铵,离子总浓度必然增大,A叙述正确;
B. b点为醋酸钠和NH3·H2O的混合液,此时NH3·H2O的电离抑制了水的电离,在d点恰好完成所有的中和反应,溶液中只有醋酸钠和醋酸铵两种溶质,两者的水解均促进水的电离,故d点水的电离程度最大,B叙述错误;
C.由于起始状态时醋酸和氢氧化钠的物质的量浓度相同,在c点,醋酸的体积是原氢氧化钠溶液体积的1.5倍,根据物料守恒可知,3c(Na+)=2c(CH3 COOH)+2c(CH3 COO-),C叙述正确;
D. 在室温下,两种弱电解质的电离常数相同。在d点溶液中只有醋酸钠和醋酸铵,且两者物质的量浓度相同。若醋酸根离子的物质的量浓度与铵根离子浓度相同,则溶液呈中性,但是,此时溶液中醋酸根离子的物质的量浓度是铵根离子的2倍,因此,醋酸根离子的水解作用大于铵根离子的水解作用,溶液呈碱性,因此,c(Na+)>c(NH![]() )>c(OH-)>c(H+),D叙述正确。
)>c(OH-)>c(H+),D叙述正确。
本题选B。

【题目】乙酸丁酯的物理性质如表。
乙酸 | 1-丁醇 | 乙酸丁酯 | |
熔点(℃) | 16.6 | -89.5 | -73.5 |
沸点(℃) | 117.9 | 117 | 126.3 |
密度(g/cm3) | 1.05 | 0.81 | 0.88 |
水溶性 | 互溶 | 可溶(9g/100g水) | 微溶 |
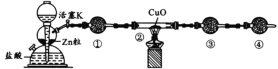
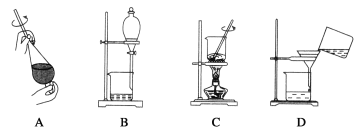
实验室用如图所示的实验装置制取乙酸丁酯。

(1)仪器A的名称___。
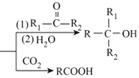
(2)写出制取乙酸丁酯的化学方程式:__。
(3)该实验中生成物除了主产物乙酸丁酯外,还可能生成的有机副产物有__(写出一种结构简式)。
(4)酯化反应是一个可逆反应,为提高1-丁醇的转化率,可采取的措施是__(写出两条)。
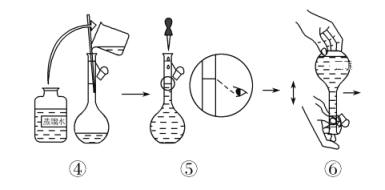
(5)从制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作,下列图示的操作中,需要的是__(填答案编号)。
(6)用60g乙酸与37g1-丁醇反应,实验中得到乙酸丁酯的质量为40.6g,则乙酸丁酯的产率为___。
【题目】CO2的富集与转化是当今环境研究的热点。
(1)化石燃料的燃烧是使大气CO2浓度增加的原因之一。汽油中含有辛烷(C8H18),1molC8H18(l)完全燃烧生成CO2(g)和H2O(l),放出5518kJ热量。写出C8H18完全燃烧的热化学方程式:__。
(2)一种富集CO2的过程如图所示。
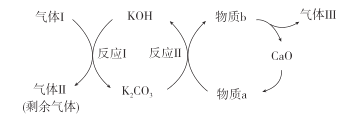
①气体Ⅰ、Ⅱ、Ⅲ中,CO2浓度最高的是___。
②反应Ⅱ的化学方程式是__。
(3)一定条件下,CO2和H2反应能生成C2H4,实现CO2向能源物质的转化。
已知:2CO2(g)+6H2(g)C2H4(g)+4H2O(g) ΔH<0
①上述反应的ΔH可根据C2H4(g)+3O2(g)=2CO2(g)+2H2O(g)和__反应的焓变计算。
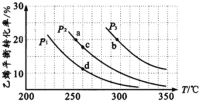
②研究温度和压强对CO2的平衡转化率的影响,结果如图所示。
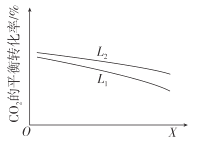
X代表的物理量是__。比较L1与L2的大小,并说明依据__。
③相同条件下,CO2和H2还能发生其它反应:
反应a:CO2(g)+H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
反应b:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
……
Fe和Co(钴)可作为该反应的催化剂。改变铁钴的物质的量比,测定相同时间内CO2的消耗率和含碳产物的占比,结果如下:
n(Fe):n(Co) | CO2消耗率/% | 含碳产物占比/% | ||
CO | C2H4 | CH4 | ||
100:0 | 1.1 | 100 | 0 | 0 |
50:50 | 30.5 | 36.8 | 20.3 | 42.9 |
0:100 | 69.2 | 2.7 | 0.2 | 97.1 |
结合数据,推测催化剂中钴的作用:__。