题目内容
【题目】实验室利用下图所示装置测定水中氢氧元素之比。下列说法错误的是
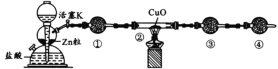
A.①、③、④中依次盛装无水CaCl2、碱石灰、碱石灰
B.需测定实验前后装置②和装置③的质量差
C.结束反应时,应先移走酒精灯,待装置②的玻璃管冷至室温,再关闭活塞K
D.实验后装置②的玻璃管中CuO未全部变红,对实验结果无影响
【答案】A
【解析】
由题中信息可知,本实验利用氧化铜质量的减少和生成水的质量关系来测定水的组成。
A. ①是用于干燥氢气和吸收挥发的氯化氢,应选择碱石灰;③用于吸收反应后生成的水,可以选择碱石灰;④是用于防止空气中的水和二氧化碳进入系统干扰实验,可以选择碱石灰,A说法错误;
B. 本实验利用氧化铜质量的减少和生成水的质量关系来测定水的组成,实验前后装置②的质量差为氧化铜所失去的氧元素的质量,实验前后装置③的质量差为氧化铜被还原后生成水的质量,因此,需测定实验前后装置②和装置③的质量差,B说法正确;
C. 结束反应时,为防止氧化铜被还原后生成铜再被氧化,装置②的固体应在氢气的保护下冷却,故应先移走酒精灯,待装置②的玻璃管冷至室温,再关闭活塞K,C说法正确;
D. 本实验利用氧化铜质量的减少和生成水的质量关系来测定水的组成,实验前后装置②的质量差为氧化铜所失去的氧元素的质量,实验后装置②的玻璃管中CuO未全部变红,对实验结果无影响,D说法正确。
本题选A。

 黎明文化寒假作业系列答案
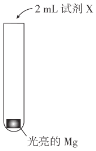
黎明文化寒假作业系列答案【题目】实验小组研究Mg与NH4Cl溶液的反应,实验如下:
| 实验 | 试剂X | 现象 |
Ⅰ | H2O | 产生极少气泡,Mg表面逐渐变暗,反应很快停止 | |
Ⅱ | 1mol/LNH4Cl溶液(pH=5) | 数分钟内持续产生较多气泡(经检验含有H2),溶液中出现大量白色固体,试管变热 |
(1)Ⅰ中Mg表面变暗,说明产生了Mg(OH)2固体。反应很快停止的原因是__。
(2)探究实验Ⅰ、Ⅱ产生气泡差异的原因。
假设一:NH4Cl溶液显酸性,c(H+)较大,与Mg反应速率较快。
①用离子方程式表示NH4Cl溶液显酸性的原因:___。
测定实验Ⅱ反应过程中溶液pH随时间的变化,结果如下:

②假设一__(填“是”或“不是”)实验Ⅰ、Ⅱ产生气泡差异的主要原因。
假设二:NH4Cl溶液中的NH![]() 溶解Mg(OH)2固体,使Mg能够持续与水反应。
溶解Mg(OH)2固体,使Mg能够持续与水反应。
进行实验:向1mol/LNH4Cl溶液中加几滴氨水,使溶液pH≈8,得到溶液a。向少量Mg(OH)2固体中加入2mL溶液a,固体溶解。
③有同学认为假设二的实验不严谨,需增加对比实验:__(填操作和现象),说明假设二正确。
④向NH4Cl溶液中加几滴氨水的目的是___。
(3)1min后,实验Ⅱ中还检测到少量NH3。
①检测NH3时要使用湿润的___试纸。
②气体中含有少量NH3的原因是__。
(4)Mg与NH4Cl溶液充分反应后,仍有大量Mg(OH)2固体生成。综合上述实验,解释Mg与NH4Cl溶液的反应比Mg与H2O的反应更剧烈的主要原因:__。