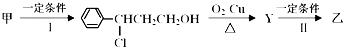题目内容
下列离子方程式正确的是( )
| A、硫酸铝溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ |
| B、明矾净水:Al3++3H2O?Al(OH)3(胶体)+3H+ |
| C、向FeI2中通入少量Cl2:2Fe2++Cl2═2Fe3++2Cl- |
| D、洗涤试管内壁的银镜:Ag+2H++NO3-═Ag++NO2↑+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.弱电解质写化学式;
B.铝离子水解生成氢氧化铝胶体;
C.氯气先氧化碘离子;
D.二者反应生成NO.
B.铝离子水解生成氢氧化铝胶体;
C.氯气先氧化碘离子;
D.二者反应生成NO.
解答:
解:A.弱电解质写化学式,离子方程式为Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故A错误;
B.铝离子水解生成氢氧化铝胶体,离子方程式为Al3++3H2O?Al(OH)3(胶体)+3H+,故B正确;
C.氯气先氧化碘离子,离子方程式为2I-+Cl2═I2+2Cl-,故C错误;
D.二者反应生成NO,离子方程式为3Ag+4H++NO3-═3Ag++NO↑+2H2O,故D错误;
故选B.
B.铝离子水解生成氢氧化铝胶体,离子方程式为Al3++3H2O?Al(OH)3(胶体)+3H+,故B正确;
C.氯气先氧化碘离子,离子方程式为2I-+Cl2═I2+2Cl-,故C错误;
D.二者反应生成NO,离子方程式为3Ag+4H++NO3-═3Ag++NO↑+2H2O,故D错误;
故选B.
点评:本题考查了离子方程式正误判断,明确离子之间发生的反应及离子方程式书写规则即可解答,注意多元弱酸根离子和多元弱碱水解离子方程式书写区别,易错选项是C,注意铁离子和碘离子还原性强弱,为易错点.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
通常人们把拆开1mol某化学键所消耗的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应物的总键能与生成物的总键能之差.
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)
Si(s)+4HCl(g),该反应的反应热△H为( )
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
| ||
| A、+412kJ?mol-1 |
| B、-412kJ?mol-1 |
| C、+236kJ?mol-1 |
| D、-236kJ?mol-1 |
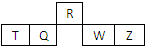 短周期元素R、T、Q、W、Z在元素周期表中的相对位置如下图所示,五种元素中只有一种金属元素.下列判断错误的是( )
短周期元素R、T、Q、W、Z在元素周期表中的相对位置如下图所示,五种元素中只有一种金属元素.下列判断错误的是( )| A、W的单质易溶于CS2 |
| B、Q与R可能形成化合物Q3R4 |
| C、T的最高价氧化物的对应水化物为强碱 |
| D、W、Z都有多种含氧酸 |
下列属于物理变化的是( )
| A、氯气溶于水 | B、食物变质 |
| C、石油的蒸馏 | D、光合作用 |
某同学将一小块金属钠投入到硫酸铜溶液中,通过此实验不能证明下列性质中的( )
| A、钠比水轻但比煤油重 |
| B、钠的熔点较低 |
| C、钠与水反应时要放出热量 |
| D、钠与水反应后溶液呈碱性 |
下列说法正确的是( )
| A、相同物质的量浓度时,溶液中c(NH4+)由大到小的顺序:NH4Al(SO4)2>NH4Cl>CH3COONH4>NH3?H2O |
| B、为了确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C、0.2mol?L-1的CH3COONa溶液与0.1mol?L-1的HCl等体积混合呈酸性:c(Na+)>c(Cl-)>c(CH3COO-)>c(H+)>c(OH-) |
| D、相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1mol/L盐酸、③0.1mol/L氯化镁溶液、④0.1mol/L硝酸银溶液中,Ag+浓度:①>④=②>③ |