题目内容
某同学将一小块金属钠投入到硫酸铜溶液中,通过此实验不能证明下列性质中的( )
| A、钠比水轻但比煤油重 |
| B、钠的熔点较低 |
| C、钠与水反应时要放出热量 |
| D、钠与水反应后溶液呈碱性 |
考点:钠的化学性质
专题:金属概论与碱元素
分析:将一小块金属钠投入到硫酸铜溶液中,钠与水先反应,产生的氢氧化钠再与硫酸铜反应生成氢氧化铜,会观察到的现象依次是:浮、熔、游、响、蓝,根据实验现象分析得出实验结论.
解答:
解:将一小块金属钠投入到硫酸铜溶液中,钠与水先反应,金属钠浮在水面上,证明钠密度比水小,金属钠熔成闪亮的小球,证明反应放热,钠的熔点低,产生蓝色氢氧化铜,说明钠与水反应后溶液呈碱性,故选A.
点评:此题是对钠与盐溶液的反应,解题的重点是对钠与水反应的有关问题,特别是物质的性质的反应的掌握,属基础性知识考查题.

练习册系列答案
相关题目
关于浓度相等的三种溶液:①H2CO3 ②NaOH ③Na2CO3溶液,下列说法正确的是( )
| A、水电离出的c(H+):③>①>② |
| B、溶液的pH:③>②>① |
| C、①和②等体积混合后的溶液:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) |
| D、①和③等体积混合后的溶液:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
下列有关说法正确的是( )
| A、一定条件下,使用催化剂能加快反应速率但不能改变平衡转化率 | ||
| B、氢氧燃料电池的能量转换形式仅为化学能转化为电能 | ||
| C、在NH4HSO4溶液中由于NH4+的水解促进了水的电离,所以水的电离程度增大 | ||
D、在一密闭容器中发生2SO2+O2?2SO3反应,增大压强,平衡会正向移动,
|
下列离子方程式书写正确的是( )
| A、用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | ||||
| B、利用腐蚀法制作印刷线路析:Fe3++Cu═Fe2++Cu2+ | ||||
C、用铜电极电解硫酸铜溶液:2Cu2++2H2O
| ||||
| D、硫酸氧钠溶液中加入氢氧化钡溶液至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
25℃时,弱酸的电离平衡常数如表:
下列有关说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1:4.3×10-7 K2:5.6×10-11 |
| A、等物质的量浓度的各溶液的pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| B、a mol/L HCN与a mol/L NaOH溶液等体积混合后所得溶液呈中性 |
| C、往冰醋酸中逐滴加水稀释,溶液导电能力始终保持减小 |
| D、在Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
下列离子方程式正确的是( )
| A、硫酸铝溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ |
| B、明矾净水:Al3++3H2O?Al(OH)3(胶体)+3H+ |
| C、向FeI2中通入少量Cl2:2Fe2++Cl2═2Fe3++2Cl- |
| D、洗涤试管内壁的银镜:Ag+2H++NO3-═Ag++NO2↑+H2O |
下面关于氢化物的叙述正确的是( )
| A、一个D2O分子所含的中子数为8 |
B、NH3的结构式为: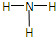 |
C、HCl的电子式为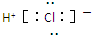 |
| D、热稳定性:HCl>HF |
下列对于“摩尔”的理解正确的是( )
| A、摩尔是国际科学界建议采用的一种物理量 |
| B、32g O2中所含氧原子数为NA个 |
| C、1mol氧约含6.02×1023个O2 |
| D、摩尔是物质的量的单位,简称摩,符号为mol |