题目内容
3.向足量H2SO4溶液中加入100mL0.4mol•L-1Ba(OH)2溶液,放出的热量是5.12kJ,如果向足量Ba(OH)2溶液中加入100mL0.4mol•L-1盐酸时,放出的热量为2.2kJ.则Na2SO4溶液与BaCl2溶液反应的热化学方程式为( )| A. | Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-2.92kJ•mol-1 | |
| B. | Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-18kJ•mol-1 | |
| C. | Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-73kJ•mol-1 | |
| D. | Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-0.72kJ•mol-1 |
分析 向H2SO4溶液中加入100mL 0.4mol•L-1 Ba(OH)2溶液反应涉及的离子方程式有Ba2+(aq)+SO42-(aq)=BaSO4(s),H+(aq)+OH-(aq)=H20(l),向足量Ba(OH)2溶液中加入100mL 0.4mol•L-1 HCl溶液时,反应涉及的离子方程式为H+(aq)+OH-(aq)=H20(l),Na2SO4溶液与BaCl2溶液反应的离子方程式为Ba2+(aq)+SO42-(aq)=BaSO4(s),从能量守恒的角度解答.
解答 解:100mL 0.4mol•L-1 Ba(OH)2的物质的量为0.04mol,向H2SO4溶液中加入100mL 0.4mol•L-1 Ba(OH)2溶液反应涉及的离子方程式有Ba2+(aq)+SO42-(aq)=BaSO4(s),H+(aq)+OH-(aq)=H20(l),100mL 0.4mol•L-1 HCl的物质的量为0.04mol,反应涉及的离子方程式为H+(aq)+OH-(aq)=H20(l),根据放出的热量为2.2kJ,
可知H+(aq)+OH-(aq)=H20(l)△H=-$\frac{2.2KJ}{0.04mol}$=-55kJ•mol-1,
设Ba2+(aq)+SO42-(aq)=BaSO4(s)△H=-QkJ•mol-1,
则0.04Q+0.08mol×55kJ•mol-1=5.12kJ,解之得Q=18,
所以Na2SO4溶液与BaCl2溶液反应的热化学方程式为Ba2+(aq)+SO42-(aq)=BaSO4(s)△H=-18kJ•mol-1.
故选B.
点评 本题考查热化学方程式的书写和反应热的计算,题目难度不大,注意从能量守恒的角度解答该题.

练习册系列答案
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
13.关于原电池说法不正确的是( )
| A. | 在铜锌原电池中Cu为正极 | |
| B. | 原电池中,化学能转变为电能 | |
| C. | 在原电池中,负极上发生氧化反应,正极上发生还原反应 | |
| D. | 在原电池中,电子从负极经过电解质溶液流向正极 |
14.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1.6g臭氧中含有氧原子的数目为0.1NA | |
| B. | 6.4g铜片被浓硫酸氧化,失去电子的数目为0.1NA | |
| C. | 标准状况下,11.2LH2O中含水分子的数目为0.5NA | |
| D. | 2 L 0.5 mol•L-1硫酸钾溶液中SO${\;}_{4}^{2-}$离子的数目为2NA |
11.生活处处有化学,下列说法正确的是( )
| A. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| B. | 用酒精、碘酒灭菌消毒是让病毒蛋白质变性死亡 | |
| C. | 煎炸食物的花生油和牛油都是可皂化的饱和酯类 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
18.下列说法正确的是( )
| A. | CH3CH2CH3在核磁共振氢谱图中能给出二种信号 | |
| B. | 氨基酸、二肽、蛋白质均既能跟强酸反应又能跟强碱反应 | |
| C. | 蔗糖、麦芽糖、硬脂酸甘油脂酸性水解都能得到2种产物 | |
| D. | 麻黄碱( )的催化氧化物能发生银镜反应 )的催化氧化物能发生银镜反应 |
8.化学与生活密切相关,下列说法不正确的是( )
| A. | 制作餐具使用的不锈钢是合金 | B. | 富含淀粉的食物可用碘水来检验 | ||
| C. | 汽油和花生油均属于酯类 | D. | 蛋白质水解的最终产物是氨基酸 |
15.下列关于铝及其化合物的说法中正确的是( )
| A. | Al2O3属于碱性氧化物 | |
| B. | 用烧碱溶液可以去除铁粉中混杂的少量铝粉 | |
| C. | Al(OH)3可治疗胃酸过多,说明铝元素超标对人体无影响 | |
| D. | 铝在空气中耐腐蚀,所以铝是不活泼金属 |
12.下图所示的实验,不能达到实验目的是(各选项中对比溶液的浓度体积均相同)( )
| 实验方案 | 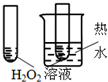 | 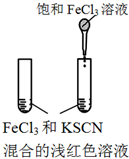 | 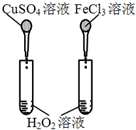 | 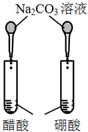 |
| 目的 | A.验证升高温度可加快H2O2分解 | B.验证增大反应物浓度对平衡的影响 | C.比较Cu2+、Fe3+对 H2O2分解速率的影响 | D.比较弱酸的 相对强弱 |
| A. | A | B. | B | C. | C | D. | D |
13.2011年,日本发生大地震并引起福岛第一核电站事故,在这国内地大部分地区空气中监测到来自日本核事故释放出的极微量人工放射性核素碘-131.有关$\underset{131}{53}$I叙述不正确的是( )
| A. | 131是这种碘-131的质量数 | B. | $\underset{131}{53}$I与$\underset{127}{53}$I互为同位素 | ||
| C. | 碘-131的中子数为53 | D. | 碘元素在周期表中位于第ⅦA族 |