题目内容
15.下列关于铝及其化合物的说法中正确的是( )| A. | Al2O3属于碱性氧化物 | |
| B. | 用烧碱溶液可以去除铁粉中混杂的少量铝粉 | |
| C. | Al(OH)3可治疗胃酸过多,说明铝元素超标对人体无影响 | |
| D. | 铝在空气中耐腐蚀,所以铝是不活泼金属 |
分析 A、氧化铝是两性氧化物;
B、铝与氢氧化钠反应,而铁不与氢氧化钠反应;
C、氢氧化铝难溶于水,但与胃酸主要成分盐酸反应会溶解生成溶于水的氯化铝和水,铝元素超标对人体有害;
D、铝因为活泼在空气中被氧化成氧化铝,而耐腐蚀.
解答 解:A、氧化铝既能与酸反应生成盐与水,又能与碱反应生成盐与水,所以氧化铝是两性氧化物,故A错误;
B、铝与氢氧化钠反应,而铁不与氢氧化钠反应,所以可以用烧碱溶液可以去除铁粉中混杂的少量铝粉,故B正确;
C、治疗胃酸过多,氢氧化铝和酸反应的离子方程式为:Al(OH)3+3H+=Al3++3H2O,铝元素超标会对人产生记忆减退,视觉与运动协调失灵,脑损伤、智力下降、严重者可能痴呆,故C错误;
D、铝因为活泼在空气中被氧化成氧化铝,而耐腐蚀,而不是不活泼,故D错误;
故选B.
点评 本题主要考查了关于铝的生活化学,掌握铝及其化合物的性质是解答的关键,题目难度不大.

练习册系列答案
相关题目
6.2013年9月在沈阳举行的第12届全运会中使用的火炬采用丙烷(C3H8)作燃料,其燃烧时发生反应的化学方程式为C3H8+5O2$\stackrel{点燃}{→}$3CO2+4H2O.下列说法中不正确的是( )
| A. | 火炬燃烧时化学能只转化为热能 | |
| B. | 所有的燃烧反应都会放出热量 | |
| C. | 1molC3H8和5molO2的总能量大于3molCO2和4molH2O的总能量 | |
| D. | 丙烷为环保型燃料 |
3.向足量H2SO4溶液中加入100mL0.4mol•L-1Ba(OH)2溶液,放出的热量是5.12kJ,如果向足量Ba(OH)2溶液中加入100mL0.4mol•L-1盐酸时,放出的热量为2.2kJ.则Na2SO4溶液与BaCl2溶液反应的热化学方程式为( )
| A. | Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-2.92kJ•mol-1 | |
| B. | Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-18kJ•mol-1 | |
| C. | Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-73kJ•mol-1 | |
| D. | Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-0.72kJ•mol-1 |
10.下列属于复合材料的是( )
| A. | 水泥 | B. | 铝合金 | C. | 天然橡胶 | D. | 玻璃钢 |
20.石油被称为工业的血液,煤被称为工业的粮食.下列说法正确的是( )
| A. | 石油和煤都是化石燃料,属于不可再生能源 | |
| B. | 煤的干馏可以得到苯、甲苯等物质,说明煤中含有苯和甲苯 | |
| C. | 石油分馏的产物如汽油、煤油等都是纯净物 | |
| D. | 石油的裂化、裂解都属于物理变化 |
7.一定条件下,在恒容密闭容器中,能表示反应X(g)+2Y(g)═2Z(g)一定达到化学平衡状态的是( )
| A. | 容器中的压强不再发生变化 | |
| B. | X、Y、Z的物质的量之比为1:2:2 | |
| C. | X、Y、Z的速率之比1:2:2 | |
| D. | 单位时间内生成n mol Z,同时消耗n mol Y |
4.下列叙述正确的是( )
| A. | NO2、SO2、BF2、NCl3分子中没有一个分子中原子的最外层电子都满足了8e-稳定结构 | |
| B. | CCl4和NH3都是以极性键结合的极性分子,P4和NO2都是共价化合物 | |
| C. | 在CaO和SiO2晶体中,都不存在单个小分子 | |
| D. | π键是由两个p电子“头碰头”重叠形成,σ键是镜面对称,而π键是轴对称 |
5.下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A. | 常温下,CH3COONa和CH3COOH混合溶液中[pH=7,c(Na+)=0.1mol•L-1]:c(Na+)=c(CH3COO-)>c(H+)=c(OH-) | |
| B. | 在O.1mol•L-1Na2C03溶液中:cc(Na+)=2c(CO32-) | |
| C. | 在O.1mol•L-1NaHC03溶液中:c(HCO3-)>c(CO32-)>c(H2C03) | |
| D. | 向0.2mol•L-1NaHC03溶液中加入等体积O.1mol•L-1NaOH溶液:c(CO32-)+c(HCO3-)+c(OH-)=c(H+)+c(Na+) |
 +2NaOH→
+2NaOH→ +2H2O.
+2H2O.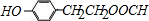 .
.